News
Ihre Auswahl
forschen, heilen / 10.11.2025
Neue Entwicklungsstörung entdeckt: Varianten des Gens UNC13A verursachen neurologische Beeinträchtigungen bei Kindern
Probleme beim Sprechen oder Laufen, Muskeln zittern und krampfen – Forschende um Noa Lipstein und Nils Brose haben in einer großen interdisziplinären Kooperation eine neue Entwicklungsstörung entdeckt, die auf Variationen im Gen UNC13A zurückzuführen ist. Die Erkenntnisse eröffnen nicht nur Behandlungsmöglichkeiten für Betroffene, sondern versprechen auch neue Ansätze für andere neurologische Erkrankungen wie Amyotrophe Lateralsklerose (ALS).
Forschende haben eine neue Entwicklungsstörung entdeckt: Varianten des UNC13A-Gens führen zu schweren neurologischen Beinträchtigungen. Das Team beschreibt drei unterschiedliche Krankheitsformen mit jeweils unterschiedlichen Symptomen mit unterschiedlichem Schweregrad, die auf verschiedenen molekularen Mechanismen beruhen. Künftig könnten sogenannte Antisense-Oligonukleotid-Therapien helfen, die Produktion krankmachender UNC13A Proteine zu unterdrücken und damit die Symptome bei zwei Formen der Krankheit abzuschwächen.
Eine E-Mail schreiben, zum Bus rennen, das Lied im Kopfhörer mitsummen – damit wir denken, fühlen oder handeln können, müssen unsere rund 100 Milliarden Nervenzellen miteinander kommunizieren. Über sogenannte Synapsen werden dabei Informationen mit Botenstoffen zwischen Zellen übertragen. Eine einzelne Nervenzelle kann bis zu 10.000 solcher Synapsen ausbilden – entsprechend zahlreich sind ihre zellulären Kommunikationspartner.
Ein Schlüsselprotein bei der synaptischen Signalübertragung ist das Protein UNC13A (Munc13-1), das daran beteiligt ist, Botenstoffe – Neurotransmitter genannt – freizusetzen. Darüber hinaus spielt UNC13A eine Rolle bei der Anpassungsfähigkeit von Synapsen, die für Lern- und Gedächtnisprozesse entscheidend ist.
Neue Entwicklungsstörung
Varianten des UNC13A‑Gens, das den Bauplan des Proteins UNC13A enthält, können zudem eine bisher unbekannte neurologische Entwicklungsstörung auslösen. Dies haben Forschende um Nils Brose vom Max-Planck-Institut für Multidisziplinäre Naturwissenschaften und Noa Lipstein, ehemals Mitarbeiterin in Broses Abteilung und jetzt Gruppenleiterin am Leibniz-Forschungsinstitut für Molekulare Pharmakologie, gemeinsam mit den klinischen Genetiker*innen Anita Rauch (Universität Zürich, Schweiz) und Reza Asadollahi (University of Greenwich, UK) entdeckt. Ihre Erkenntnisse wurden jüngst in der Zeitschrift Nature Genetics veröffentlicht.
Im Rahmen weltweiter Kooperationen mit zahlreichen Kliniken identifizierte das Team bislang rund 50 Patient*innen, bei denen dieses Syndrom diagnostiziert wurde. Viele von ihnen haben so eine Erklärung für ihr Krankheitsbild erhalten.Das Spektrum der Beeinträchtigungen durch das veränderte Gen reicht dabei von verzögerter Entwicklung und geistigen Beeinträchtigungen über Sprach- und Bewegungsstörungen bis hin zu Zittern und Krampfanfällen. In einigen Fällen kommt es auch zum Tod im frühen Kindesalter.
Drei Formen der Entwicklungsstörung
Die Abteilung Molekulare Neurobiologie von Nils Brose erforscht seit vielen Jahren die Wirkweise des Proteins UNC13A. Nur diese langjährigen Anstrengungen ermöglichten es, die Ursachen der Entwicklungsstörung auf molekularer Ebene zu entschlüsseln. Mithilfe elektrophysiologischer Studien an Mäusen und dem Fadenwurm C. elegans konnte das Forschungsteam aufklären, wie sich verschiedene Varianten des UNC13A- Gens auf die Funktion von Nervenzell-Synapsen auswirken. In bislang 20 Fällen ist es auf diese Weise gelungen, die Krankheitsursachen aufzuklären.
„Die Symptome variieren, je nachdem, welche Funktion das UNC13A-Protein nicht mehr ausüben kann“, erklärt Lipstein. „Die krankheitsauslösenden Genvarianten lassen sich in drei Subtypen der Erkrankung zusammenfassen, bei denen jeweils andere Beeinträchtigungen von Nervenzellen auftreten. Sie rufen jeweils ein eigenes Krankheitsbild hervor und erfordern daher unterschiedliche therapeutische Ansätze, obwohl die Ursache im selben Gen liegt“, betont die Wissenschaftlerin.
Ansätze für neue Therapien
Die Ergebnisse der Forschenden machen Hoffnung für Therapien: „Antisense-Oligonukleotid-Therapien, die die Produktion krankmachender Proteine unterdrücken und so die relative Häufigkeit des normalen UNC13A-Proteins erhöhen, könnten die Krankheitssymptome bei zwei Formen der Entwicklungsstörung verringern“, sagt Brose. Die neuen Erkenntnisse können zudem Wege eröffnen, um häufigere neurologische Erkrankungen wie ALS, Frontotemporale Demenz (FTD) und die Alzheimer- Krankheit zu behandeln. Jüngste Studien zeigten, dass eine veränderte Produktion des UNC13A-Proteins ein Schlüsselfaktor für das Fortschreiten dieser Krankheiten ist.
„Unsere Studien machen den Wert langfristiger Grundlagenforschung deutlich. Die Identifizierung der genauen molekularen Grundlagen dieser neurologischen Entwicklungsstörung ist ein entscheidender Schritt zur Entwicklung von Behandlungsmethoden“, betont Lipstein.
Publikation: Asadollahi, R., Ahmad, A., Boonsawat, P. et al. Pathogenic UNC13A variants cause a neurodevelopmental syndrome by impairing synaptic function. Nat Genet (2025). https://doi.org/10.1038/s41588-025-02361-5
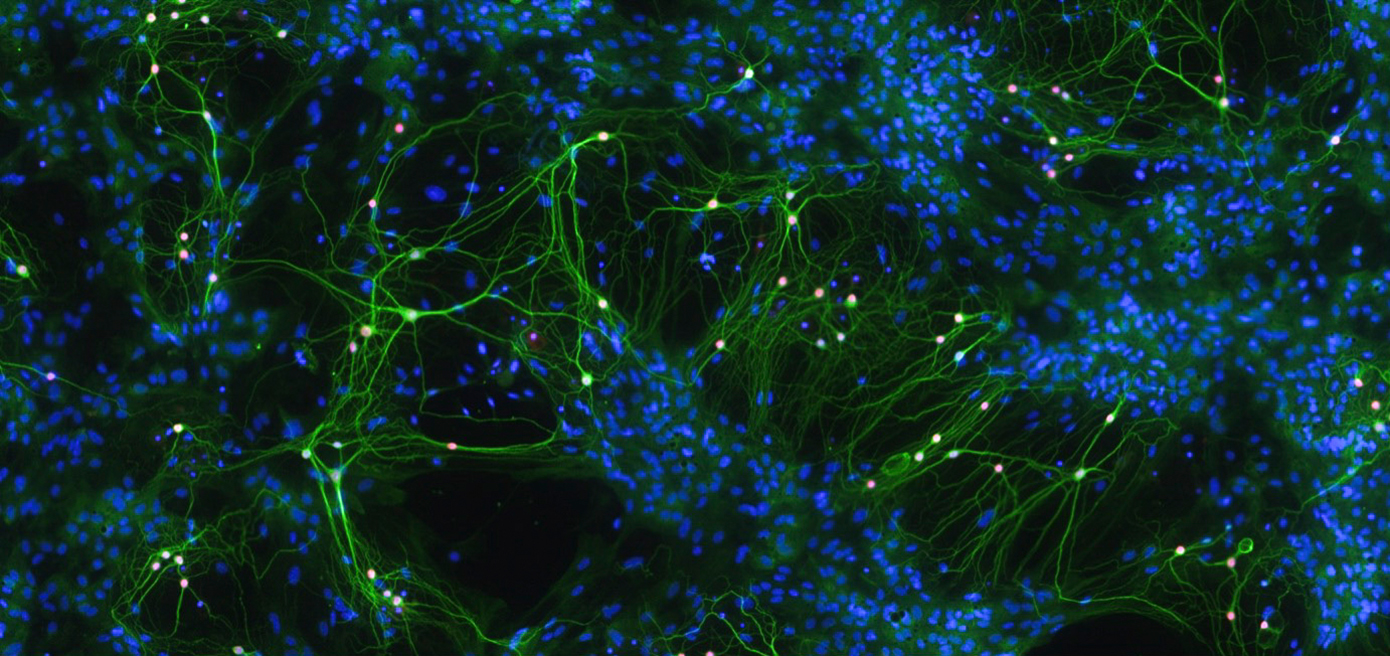
Abbildung: Nervenzellen (grün) bilden neuronale Netzwerke, in denen Informationen übertragen werden. Fehler in dieser Kommunikation können zu neurodegenerativen, neurologischen und neuropsychiatrischen Erkrankungen führen.
© Pia Venneker
Gemeinsame Pressemitteilung des Leibniz-Forschungsinstitut für Molekulare Pharmakologie und des Max-Planck-Instituts für Multidisziplinäre Naturwissenschaften
Quelle: PRESSEMITTEILUNG des Leibniz-Forschungsinstituts für Molekulare Pharmakologie (FMP) im Forschungsverbund Berlin e.V.Alle News im Überblick
News Buch Berlin
T-knife Therapeutics Announces Authorization of Clinical Trial Application for TK-6302, A Multi-Armored, CRISPR based T cell Therapy for Solid Tumors
Phase 1 ATLAS trial to evaluate TK-6302 in patients with advanced PRAME-positive solid tumors authorized for initiation
weiter ...Unterschiedliche Rollen für zwei ähnliche Enzyme
Zwei eng verwandte Enzyme, MNK1 und MNK2, spielen im Gehirn sehr unterschiedliche Rollen und regulieren jeweils ein anderes Verhalten. Wie Forschende vom Max Delbrück Center in „Molecular Psychiatry“ ...
weiter ...Weichen stellen, um Innovationskraft zu sichern
Landespolitik besuchte den Campus Berlin-Buch anlässlich der IHK-Roadshow zum Gesundheitsstandort Berlin 2030
weiter ...Termine Buch Berlin
18.03.2026, 08:30
/ Campus Berlin-Buch
vocatium Berlin focus 2026: Fachmesse für Ausbildung+Studium
Entdecke berufliche Möglichkeiten, informiere dich und sprich mit Expert:innen über Einstieg, Voraussetzungen und Bewerbung.
weitere Informationen20.03.2026, 08:45
Einladung: UniStem Day für Berliner Schülerinnen und Schüler aus Biokursen
Das German Stem Cell Network (GSCN) lädt die an Biologie interessierten Berliner Schülerinnen und Schüler (Biologie-Leistungskurse und Grundkurse) mit ihren Lehrkräften herzlich zum UniStem Day – zum ...
weitere Informationen22.09.2026, 09:00
/ Campus Berlin-Buch
GMP Biotech Summer School
Knowing and applying the Good Manufacturing Practice (GMP) regulations is one of the key elements in the manufacture of medicinal products for clinical trials and on an industrial level.
weitere Informationen







