Aktuelles
forschen, produzieren, heilen, bilden / 28.05.2026
Virtual Reality, Videomapping und eine begehbare Vene

VR-Exkursionen zu Mikroplastik im Gehirn, eine begehbare Vene oder das Labor als Escape-Room: Mit rund 70 Angeboten ist das Max Delbrück Center bei der Langen Nacht der Wissenschaften dabei. Die Forschenden zeigen allen Interessierten vor Ort, wie ihre Arbeit die Medizin von morgen prägen wird.
Der Countdown bis zur Langen Nacht der Wissenschaften läuft! Ab 17 Uhr öffnen am 6. Juni das Max Delbrück Center auf dem Campus Buch und das MDC-BIMSB in Mitte ihre Labore und Gebäude für Gäste jeden Alters.
Einige Höhepunkte des Programms:
Die begehbare Vene – Die Venen transportieren sauerstoffarmes Blut zurück zum Herzen, meist gegen die Schwerkraft. Ähnlich wie die Arterien können sie verstopfen. Aber wie sieht eine Vene aus? Gemeinsam mit Expert*innen können Gäste ein sechs Meter langes begehbares Venenmodell erkunden und sich dabei über unsere Forschung informieren. Max Delbrück Center, Campus Buch, Foyer des MDC.C, 16:00 bis 23:00 Uhr.
Vom Modell zum Menschen – Was passiert während einer klinischen Studie? Wie schlägt man die Brücke zwischen experimenteller und klinischer Forschung? Diese Fragen beantworten Wissenschaftler*innen aus der AG Dechend / Müller allen Interessierten am Beispiel der Herz-Kreislauf-Erkrankungen. An ihrem Stand können Gäste unter anderem mittels Virtual Reality das Herz erkunden. Max Delbrück Center, Foyer des MDC.C, 17:00 bis 22:00 Uhr.
Escape-Room – Wie ist es, als Molekularbiolog*in in einem Labor zu arbeiten? Wir laden Sie ins Landthaler-Labor ein und machen daraus einen Escape-Room. Bei diesem immersiven Erlebnis erfahren Gäste mehr über unsere experimentellen Methoden und arbeiten als Team zusammen, um einem unbekannten Virus seine Geheimnisse zu entlocken. Max Delbrück Center, MDC-BIMSB, Anmeldung am Infopunkt im Erdgeschoss, 17:00, 18:30, 20:00 und 21:30 Uhr (DE und EN).
Expeditionen ins Gehirn
Mikroplastik ist praktisch überall. Doch was passiert, wenn es ins Gehirn gelangt? Das ist eine von vielen Fragen, die am Max Delbrück Center mithilfe von Hirn-Organoiden, Einzelzelltechnologien und aufwendigen lichtmikroskopischen Aufnahmen bearbeitet werden. Während der Langen Nacht wird das Thema bei zwei Angeboten angerissen:
Mini-Gehirne und Big Data – Organoide bilden die zelluläre Komplexität menschlicher Organe in der Petrischale in 3D nach: Die Organoid-Technologieplattform und die AG Rajewsky untersuchen Organoide und 3D-Zellkulturen aus Tumorgewebe mit räumlicher Transkriptomik und bioinformatischen Werkzeugen. So können sie Krankheitsmechanismen oder auch die Auswirkungen von Mikroplastik aufdecken. Max Delbrück Center, MDC-BIMSB, Anmeldung am Infopunkt im Erdgeschoss, 17:00, 19:00 und 21:30 Uhr (DE).
Eintauchen in die Lichtmikroskopie – Gäste können lichtmikroskopische Aufnahmen unter anderem zu aktueller Mikroplastik-Forschung anschauen. Und zwar nicht in 2D am Bildschirm: Vielmehr tauchen sie mit Virtual-Reality-Brillen tief in die Bilder ein und betrachten Nerven- und andere Zellen aus völlig neuen Blickwinkeln. Max Delbrück Center, MDC-BIMSB, Treppenhaus, 17:00 bis 22:30 Uhr (DE und EN).
Spaghetti im Gehirn – Was geht in unserem Gehirn vor sich, wenn wir an Alzheimer erkranken? Die AG Birol zeigt, wie die Forschenden den Ausbruch und das Fortschreiten neurodegenerativer Erkrankungen anhand von Gehirn-Organoiden besser verstehen wollen – und dabei mitunter auf Spaghetti-ähnliche Proteine stoßen. Gäste haben die Möglichkeit, Neuronen unter dem Mikroskop zu betrachten und deren Aktivität mit eigenen Augen zu verfolgen. Max Delbrück Center, MDC-BIMSB, Anmeldung am Infopunkt im Erdgeschoss, 17:30 und 19:00 Uhr (EN).
Unter dem Sternenhimmel
Pubquiz mit Tom & Darren – Das vielfältige Quiz zum Mitmachen: Gäste spielen in kleinen Teams miteinander und stellen sich Fragen zu Alltags‑, Allgemein- und Spezialwissen. Max Delbrück Center, Campus Buch, Wiese am blauen Bären, 22:15 bis 23:15 Uhr (DE).
Kunst und Kultur über den Dächern Berlins – Wer zwischendurch auf andere Gedanken kommen will, ist auf der Dachterrasse des MDC-BIMSB richtig: Von 20 bis 22 Uhr legt dort DJ d0erte elektronische Musik auf. Und von 21 bis 23 Uhr zeigt Alexandra Huchet (onetwothreesun) ihre abstrakte Videomapping-Kunst, auch mit wissenschaftlichen Bildern. Max Delbrück Center, MDC-BIMSB, Dachterrasse, 20:00 bis 23:00 Uhr.
Tickets: Der Berlin-weite Eintritt kostet 7,50 Euro. Kinder unter sechs Jahren haben wie immer freien Eintritt.
Standorte: Campus Berlin-Buch, Robert-Rössle-Straße 10, 13125 Berlin. MDC-BIMSB, Hannoversche Straße 28, 10115 Berlin.
Weitere Informationen
27.05.2026
Spaß mit Experimenten, Labor zum Anfassen und Staunen bei der Zaubershow für Kinder

Faszination Naturwissenschaften: Zur Langen Nacht der Wissenschaften am 6. Juni lädt das Gläserne Labor auf dem Campus Berlin-Buch gemeinsam mit dem Forschergarten, Partnerschulen und Stiftungen Familien mit Kindern zum Mitmachen ein.
Was bedeutet eigentlich Vortexen und wie funktioniert eine Pipette? Wer gern einmal Labortechniken ausprobieren möchte, ist im Open Lab herzlich willkommen. In Experimentierkursen und Mitmachexperimenten erfahren die Teilnehmenden unter anderem, wie das Immunsystem funktioniert, wie sich die seltene Schmetterlingskrankheit anfühlt, welche Chemie in Geheimtinte steckt, wann sich Schiffe versenken lassen und wie es den Flimmerhärchen der Lunge beim Rauchen geht. Zwei Experimentalshows werden das Publikum verzaubern, ganz neu ist Oliver Grammels anziehende Zauberei mit Physik.
Highlights aus dem Programm:
Open Lab: Das Labor zum Anfassen & Probieren
Sie waren noch nie in einem Forschungslabor? Dann ist diese Tour genau das Richtige: Gemeinsam mit Wissenschaftler:innen besuchen Sie eines unserer Forschungslabore und probieren typische Arbeitsschritte wie Pipettieren, Vortexen, Zentrifugieren und vieles mehr. Vor Ort können Sie mit unseren Forschenden ins Gespräch kommen, mehr über ihre Forschungsthemen und Experimente erfahren – und verstehen, warum Rückschläge im Forschungsalltag keine Seltenheit sind.
Erwin-Negelein-Haus (D79), Erdgeschoss, Leibniz-Forschungsinstitut für Molekulare Pharmakologie & Gläsernes Labor, ohne Anmeldung, durchgängig geöffnet
→ MITMACHEXPERIMENTE
Dein Körper. Deine Fragen. Unsere Forschung.
Wie funktioniert das Immunsystem? Was passiert im Gehirn beim Lernen? Und warum sind manche Erkrankungen so selten, dass kaum jemand von ihnen gehört hat? Das Deutsche Zentrum für Kinder- und Jugendgesundheit (DZKJ) lädt Kinder, Jugendliche und ihre Familien ein, Gesundheitsforschung hautnah zu erleben. An sieben Mitmach-Stationen warten spielerische Aktionen für alle Altersgruppen. Lösen Sie alle sieben Aufgaben und freuen Sie sich über eine kleine Überraschung!
Erwin-Negelein-Haus (D79), Erdgeschoss, für Grundschulkinder, Deutsches Zentrum für Kinder- und Jugendgesundheit (DZKJ), Stempelstation für Forscherdiplom, ohne Anmeldung, 17:00 bis 22:00 Uhr
Rauchende Wimpertierchen
Was passiert mit den Flimmerhärchen in der Lunge, wenn wir rauchen? Dies können Sie in einem anschaulichen Versuch im Gläsernen Labor herausfinden.
Max Delbrück Communications Center (MDC.C), ab 12 Jahren, Gläsernes Labor, Anmeldung am Infopunkt im MDC.C., 18:00, 19:30 Uhr
Gesundes Herz und gesunde Gefäße – gute Durchblutung!
Finde heraus, wie oft dein Herz in einer Minute schlägt, wie hoch dein Blutdruck ist und welche Menge an Sauerstoff in deinem Blut vorhanden ist. Mikroskopiere einen Blutausstrich und schau dir das schlagende Herz von Wasserflöhen an!
Experimentierhalle in der Mensa, Haus 14, für Grundschüler und deren Eltern, Partnerschule Robert-Havemann-Gymnasium, Stempelstation für Forscherdiplom, 16:00 – 22:00 Uhr
Abenteuer Mikrokosmos
Entdecke faszinierende Pflanzenwelten unter dem Mikroskop beim künstlerischen Zeichnen-Workshop mit Illustratorin und Künstlerin Yi Meng Wu.
Gläsernes Labor (A13), Dachgeschoss, ab 6 Jahren, 17:30 – 19:30 Uhr
Seltene Erkrankungen selbst erleben
Zahlreiche Erkrankungen sind für Betroffene mit großen Einschränkungen verbunden. Finden Sie hautnah heraus, wie sich die Schmetterlingskrankheit anfühlt und erfahren Sie mittels einer Simulation, wie sich die Sehleistung bei z.B. „grünem Star“, „grauem Star“ sowie Netzhautablösung verändert. Wir zeigen, mit welchen Beeinträchtigungen viele Menschen leben müssen und was es für den Alltag bedeutet.
Erwin-Negelein-Haus (D79), Erdgeschoss, Berliner Sparkassenstiftung Medizin, Stempelstation für Forscherdiplom, 17:00 bis 22:00 Uh
Schiffe versenken
Wie viel Ladung kann ein Schiff eigentlich tragen – und warum geht es nicht sofort unter? Hier testet ihr verschiedene Schiffsformen und untersucht, welche Bauweise besonders viel Gewicht aushält, bevor sie sinkt. Spielerisch experimentiert ihr mit Wasser, Gewichten und unterschiedlichen Rumpfformen – und entdeckt dabei spannende physikalische Phänomene.
Kommt vorbei, probiert es aus und werdet selbst zu kleinen Schiffbauingenieur:innen!
Experimentierhalle in der Mensa, Haus 14, für Grundschulkinder, Partnerschule Käthe-Kollwitz Gymnasium Berlin, 16:00 bis 20:00 Uhr
Das Geheimnis der wandernden Farben
Entdeckt spielerisch ein spannendes wissenschaftliches Prinzip: Durch das Zusammenspiel von Feuchtigkeit und Zucker entstehen faszinierende Muster und Farben. Experimentiert selbst und findet heraus, wie sich Zucker verhält, wenn er mit Wasser in Berührung kommt – und lasst kleine Kunstwerke entstehen.
Experimentierhalle in der Mensa, Haus 14, für Grundschulkinder, Forschergarten & Gläsernes Labor, 16:00 bis 22:00 Uhr
→ SCIENCE ENTERTAINMENT
Rettungsmission im All
Qualm, Laser, Schnee: Ein Potpourri von Experimenten erwartet Groß und Klein bei der Experimentalvorlesung des Schülerforschungszentrum Pankow am Robert-Havemann-Gymnasium.
Experimentierhalle in der Mensa, Haus 14, für die ganze Familie, ohne Anmeldung, 17:00, 19:00 Uhr
Wissen-schafft-Spaß – Mag(ie)netisch: Phantastische Physik - anziehende Zauberei
Metall bremst sich wie von selbst, Dinge schweben, Kräfte wirken ohne Berührung. Magie? …oder doch Physik? Zauberkünstler und Biochemiker Oliver Grammel bietet in seiner überraschenden und lehrreichen Show Wissenschaftsspaß für alle.
Max Delbrück Communications Center (MDC.C) (C83), Axon 1, für die ganze Familie, ohne Anmeldung, 17:30, 19:00, 20:30 Uhr
Zum gesamten Programm des Gläsernen Labors: https://www.glaesernes-labor.de/de/lndw-2026
forschen, produzieren, heilen / 22.05.2026
Berlin zeichnet herausragende Deep-Tech-Unternehmen aus – darunter MyoPax

In diesem Jahr wurde erstmalig ein Deep Tech Award in der Kategorie Bio- & Healthtech vergeben. Gewinner ist MyoPax, ein Spin-off des Max Delbrück Center und der Charité – Universitätsmedizin Berlin, das seinen Ursprung auf dem Campus Berlin-Buch hat.
KI-gestützte Faktenchecks gegen Desinformation, neuartige Zelltherapien zur Regeneration von Muskelgewebe, nachhaltiger 3D-Druck oder dezentrale Satellitenkommunikation: Am Mittwochabend, 20. Mai 2026, hat die Senatsverwaltung für Wirtschaft, Energie und Betriebe fünf herausragende Berliner Unternehmen mit dem Deep Tech Award ausgezeichnet. Damit würdigt sie bereits im elften Jahr in Folge technologische, forschungsbasierte Innovationen aus Berlin, die durch Anwendungsnähe und gesellschaftliche Relevanz und Mehrwert überzeugen. Die feierliche Preisverleihung mit Wirtschaftssenatorin Franziska Giffey sowie Michael Biel, Staatssekretär für Wirtschaft, fand erstmals im Rahmen der Deep Tech Momentum-Konferenz in den Wilhelm Studios in Berlin statt.
Franziska Giffey, Bürgermeisterin und Senatorin für Wirtschaft, Energie und Betriebe: „Wir wollen Berlin zum Innovationsstandort Nr. 1 in Europa machen. Die heute ausgezeichneten Unternehmen bringen technologische Spitzenforschung in die konkrete Anwendung und bieten Lösungen für aktuelle Herausforderungen. Damit zeigen sie eindrucksvoll, wie viel Innovationskraft in Berlin steckt. Mit dem Deep Tech Award würdigen wir den Mut und die Exzellenz unserer Gründerinnen und Gründer. Durch die neue Partnerschaft mit der Deep Tech Momentum-Konferenz schaffen wir zudem eine Bühne, die Berlins klügste Köpfe noch enger mit Kooperationspartnern aus der Industrie sowie internationalen Investorinnen und Investoren vernetzt. Damit sichern wir nachhaltiges Wachstum und technologische Souveränität am Standort Berlin.“
Der Deep Tech Award ist mit insgesamt 50.000 Euro dotiert und wird in fünf Kategorien vergeben: „Advanced Manufacturing“, „Bio- & Healthtech“, „Künstliche Intelligenz“, „Quantentechnologien, Photonik & Mikroelektronik“ sowie „Web3 & Distributed Ledger Technologies (DLT)“. Aus über 84 Bewerbungen zeichneten Fachjurys fünf Gewinnerunternehmen aus, die jeweils ein Preisgeld von 10.000 Euro erhalten.
Mit der erstmaligen Einbindung des Deep Tech Awards im Rahmen der Deep Tech Momentum wird der Preis noch stärker international positioniert. Die Konferenz gilt als eine der führenden europäischen Plattformen zur Vernetzung von Deep-Tech-Startups mit Unternehmen und Investor:innen. Die neue Partnerschaft unterstreicht den Anspruch des Awards, Berlins innovativste Technologieunternehmen nicht nur zu würdigen, sondern sie zugleich noch enger mit dem europäischen Innovationsökosystem zu vernetzen. In diesem Rahmen wurde in diesem Jahr auch erstmals der Sonderpreis „Deep Tech Award for Breakthrough Momentum“ verliehen. Er richtet sich an von Deep Tech Momentum kuratierte europäische Startups, die exzellente wissenschaftliche Innovation mit außergewöhnlichem Skalierungspotenzial verbinden.
Die Gewinner:innen des Deep Tech Award 2026 auf einen Blick:
Deep Tech Star der Kategorie „Advanced Manufacturing”: Endless Industries GmbH
Endless Industries revolutioniert die Fertigung aus Faserverbundstoffen — also Materialien, bei denen Kohlenstofffaser in ein bindendes Harz eingebettet sind — durch eine 3D-Druck-Lösung. So können aufwendige und teure Herstellungsprozesse ersetzt und Abfall eingespart werden.
Website: www.endless.industries
Deep Tech Star in der Kategorie „Bio-& Healthtech”: MyoPax GmbH
Im Zentrum der Arbeit von MyoPax stehen neuartige Zelltherapien und Genkorrekturen zur Regeneration von Muskelgewebe. Damit adressiert das Unternehmen insbesondere schwere Muskelverletzungen und -erkrankungen und eröffnet Patient:innen vielversprechende neue Behandlungsperspektiven.
Website: www.myopax.com
Deep Tech Star in der Kategorie „Künstliche Intelligenz ”: Gretchen AI GmbH
Gretchen AI entwickelt modernste KI zur Erkennung von Deepfakes und Fake News und kann deren Verbreitungshistorie rekonstruieren. Damit ermöglicht das Berliner Unternehmen großen Medienhäusern bis zu sechsmal schnellere Faktenchecks bei gleichbleibender Zuverlässigkeit – ein entscheidender Beitrag zur Sicherung des öffentlichen Informationsraums.
Website: www.gretchen-ai.com
Deep Tech Star in der Kategorie „Quantentechnologien, Photonik & Mikroelektronik”: Xavveo GmbH
Xavveo entwickelt photonische Radarsensoren, die in Bereichen wie Navigation und Messtechnik neue Maßstäbe setzen, etwa bei der Umfelderkennung von Autos. Die Technologie ermöglicht eine bislang unerreichte Präzision und hat das Potenzial, bestehende Sensorlösungen in einer Vielzahl von Industrien grundlegend zu ersetzen.
Website: www.xavveo.com
Deep Tech Star in der Kategorie „Web3 & Distributed Ledger Technologies (DLT)”: Decen Space UG
Das Startup Decen Space entwickelt ein dezentrales Koordinationsnetzwerk aus Soft- und Hardwarekomponenten für die sichere und effiziente Synchronisierung von Datenströmen zwischen Satelliten und Bodenstationen. Mit dieser Lösung werden höhere Datenübertragungsraten bei deutlich geringeren Kosten ermöglicht, zudem werden für Satellitenbetreiber mehr Kontaktzeiten zu ihren Satelliten ermöglicht.
Website: www.decenspace.com
Deep Tech Star des Sonderpreises “Deep Tech Award for Breakthrough Momentum”: Six Robotics AS
Six Robotics AS ist ein norwegisches Unternehmen, das sich auf die Entwicklung von Autonomie-Software für Flotten unbemannter Luftfahrzeuge spezialisiert hat. Die Software basiert auf innovativen Schwarmintelligenz-Algorithmen und Echtzeit-Mission-Steuerungsarchitekturen, die eine hohe Autonomie und Effizienz der Fluggeräte gewährleisten. Damit ermöglicht das Unternehmen Drohnen, Missionen als intelligente Teams zu koordinieren und auszuführen. Dadurch wird der Einsatz vernetzter autonomer Systeme in modernen Verteidigungseinsätzen vorangetrieben.
Website: www.sixrobotics.com
Weitere Informationen über den Deep Tech Berlin und den Deep Tech Award finden Sie unter: www.berlin.de/deeptech/
Quelle: Pressemitteilung der Senatsverwaltung für Wirtschaft, Energie und Betriebe.
produzieren / 22.05.2026
Eckert & Ziegler erhält erneut „Best Managed Companies Award“
Die Eckert & Ziegler SE (ISIN DE0005659700) ist zum dritten Mal in Folge Preisträger des „Best Managed Companies Award“. Mit dieser Auszeichnung würdigen Deloitte Private, UBS, die Frankfurter Allgemeine Zeitung und der Bundesverband der Deutschen Industrie (BDI) hervorragend geführte, mittelständische Unternehmen.
„Gute Unternehmensführung ist gerade in wirtschaftlich schwierigen Zeiten von zentraler Bedeutung. Der Best Managed Companies Award ist eine verdiente Auszeichnung für Unternehmen, die Verantwortung, Weitsicht und nachhaltiges Handeln erfolgreich miteinander verbinden“, sagt Tobias Vogel, CEO UBS Europe SE.
„Diese Auszeichnung ist für uns Anerkennung und Ansporn zugleich. Sie bestätigt, dass wir mit einer klaren Strategie im Wachstumsmarkt Nuklearmedizin auf dem richtigen Weg sind – und das gemeinsam mit einem großartigen Team weltweit,“ ergänzt Dr. Dirk W. Becker, Mitglied der Konzernleitung der Eckert & Ziegler SE, der den Unternehmenspreis im Rahmen einer feierlichen Veranstaltung in Frankfurt am Main entgegennahm.
Im Rahmen eines mehrstufigen Bewerbungsverfahrens wurden die teilnehmenden Unternehmen auf ihre Exzellenz in den folgenden Kernbereichen bewertet: Strategie, Produktivität und Innovation, Kultur und Commitment sowie Finanzen und Governance. Voraussetzung für die Auszeichnung ist eine hohe Performance in allen vier Bereichen. Danach wurden die Preisträger von einer Jury, bestehend aus renommierten Vertretern aus Wirtschaft, Wissenschaft und Medien ausgewählt.
Über Eckert & Ziegler
Die Eckert & Ziegler SE gehört mit über 1.000 Mitarbeitern zu den führenden Anbietern von isotopentechnischen Komponenten für Nuklearmedizin und Strahlentherapie. Das Unternehmen bietet weltweit an seinen Standorten Dienstleistungen und Produkte im Bereich der Radiopharmazie an, von der frühen Entwicklung bis hin zur Kommerzialisierung. Die Eckert & Ziegler Aktie (ISIN DE0005659700) ist im TecDAX der Deutschen Börse gelistet.
Wir helfen zu heilen.
leben, heilen, bilden / 21.05.2026
Die Roadshow des Helios Clusters Berlin-Brandenburg hat begonnen

Mit großem Interesse ist die gemeinsame Roadshow der drei Helios Kliniken des Clusters Berlin-Brandenburg, bestehend aus dem Helios Klinikum Berlin-Buch, dem Helios Klinikum Emil von Behring und dem Helios Klinikum Bad Saarow, gestartet. Mitarbeitende des Helios Klinikums Emil von Behring läuteten die Tour durch die Region ein. Im Shoppingcenter Das Schloss in Berlin-Steglitz informierten sie über medizinische Angebote sowie berufliche Perspektiven und boten Besucher:innen Mitmachaktionen wie unter anderem ein Speeddating mit dem Leitungsteam, das Zunähen von Schnitten mit dem Team der Klinik für Allgemein-, Viszeral und Minimalinvasive Chirurgie sowie eine Teddyklinik für Kinder.
Im Zeitraum vom 20. Mai bis 20. Juni 2026 laden Mitarbeitende des Helios Klinikums Berlin-Buch, Helios Klinikums Emil von Behring und des Helios Klinikums Bad Saarow Interessierte in insgesamt fünf Shoppingcentern ein, Gesundheit aktiv in den eigenen Alltag zu integrieren, Vorsorge neu zu entdecken und sich über Karriere- sowie Ausbildungsmöglichkeiten bei Helios auszutauschen.
Unter dem Motto „Finde, was zu dir passt. Für deine Gesundheit. Für deine Karriere“ erwartet die Besucher:innen ein abwechslungsreiches Programm mit Einblicken in unterschiedliche medizinische Fachbereiche und den Klinikalltag. Das Informationsangebot richtet sich dabei gleichermaßen an Patient:innen, Bewerber:innen und Interessierte. Vor Ort stehen Fachkräfte aus verschiedenen Bereichen für Fragen und persönliche Gespräche zur Verfügung. So etwa Pflegekräfte, Ärzt:innen, Therapeut:innen, Hebammen und Mitarbeitende aus dem Recruiting. Ergänzt wird das Angebot durch wechselnde Themenschwerpunkte und Mitmachaktionen für die ganze Familie rund um Gesundheit, Prävention und medizinische Versorgung.
Erst shoppen, dann bei Deutschlands größtem privaten Klinikbetreiber durchstarten: Die Roadshow findet stets während der Öffnungszeiten des jeweiligen Centers statt.
Die Termine im Überblick:
1. Das Schloss in Berlin-Steglitz vom 20. bis 23. Mai 2026 mit dem Helios Klinikum Emil von Behring
2. Rathaus Center Pankow vom 27. bis 30. Mai 2026 mit dem Helios Klinikum Berlin-Buch
3. A10 Center Wildau vom 03. bis 06. Juni 2026 mit dem Helios Klinikum Bad Saarow
4. Linden-Center vom 10. bis 13. Juni 2026 mit dem Helios Klinikum Berlin-Buch
5. Stern-Center Potsdam vom 17. bis 20. Juni 2026 mit dem Helios Klinikum Emil von Behring
An ausgewählten Nachmittagen erwarten die Besucher:innen in den Centern zudem besondere Programmpunkte aus verschiedenen medizinischen Fachrichtungen, darunter Kinder- und Jugendmedizin, Pflege, Geburtshilfe oder moderne diagnostische und therapeutische Verfahren. Nach dem erfolgreichen Start der Roadshow in Berlin-Steglitz geht es ab dem 27. Mai 2026 mit dem Team des Helios Klinikums Berlin-Buch im Rathaus Center Pankow weiter.
Die genauen Termine und Standorte sowie weitere Informationen werden fortlaufend auf der Landingpage der Roadshow veröffentlicht.
Über Helios
Helios verbessert mit dem Clusteransatz die medizinische Qualität für Patienten, indem Kompetenz gebündelt und das Netzwerk intensiviert wird. Zum Cluster Berlin-Brandenburg gehören das Helios Klinikum Berlin-Buch, das Helios Klinikum Emil von Behring und das Helios Klinikum Bad Saarow.
Das Helios Klinikum Berlin-Buch ist ein Krankenhaus der Maximalversorgung mit über 1.000 Betten, mehr als 60 Kliniken, Instituten und spezialisierten Zentren. Schwerpunkte sind zertifizierte Zentren für Brust-, Darm- und Hauttumore, Frühgeborene und akute Gefäßerkrankungen. Das Klinikum ist zudem als "Klinik für Diabetiker geeignet DDG" ausgezeichnet.
Das Helios Klinikum Emil von Behring ist mit über 500 Betten eines der größten Krankenhäuser mit qualifizierter Schwerpunktversorgung im Berliner Südwesten. Insbesondere die Klinik für Orthopädie und Unfallchirurgie steht für moderne, innovative und patientenorientierte Versorgung auf höchstem Niveau.
Das Helios Klinikum Bad Saarow ist mit rund 630 Betten ein Krankenhaus der qualifizierten Regelversorgung und zählt zu den modernsten Kliniken der Region. Mit 19 Fachabteilungen, mehreren Instituten, einer Zentralen Notaufnahme und zertifizierten Zentren bietet es umfassende Diagnostik und Therapie.
In Deutschland betreibt Helios mehr als 80 Kliniken, rund 200 Medizinische Versorgungszentren (MVZ), sechs Präventionszentren und 30 arbeitsmedizinische Zentren. Helios behandelt im Jahr 2025 rund 5,6 Millionen Menschen in Deutschland, davon mehr als 4 Millionen ambulant. Seit seiner Gründung setzt Helios auf messbare, hohe medizinische Qualität und Datentransparenz und ist bei über 90 Prozent der Qualitätsziele besser als der bundesweite Durchschnitt. In Deutschland beschäftigt Helios rund 80.000 Mitarbeitende und erwirtschaftete im Jahr 2025 einen Umsatz von rund 8,1 Milliarden Euro. Helios steht mit 35 eigenen Bildungszentren für Aus-, Fort- und Weiterbildung im Gesundheitswesen. Sitz der Unternehmenszentrale ist Berlin.
Fresenius Helios ist der führende private Gesundheitsdienstleister in Europa und versorgt mit rund 140 Kliniken und zahlreichen ambulanten Einrichtungen jährlich rund 27 Millionen Menschen. Zusammen mit Fresenius Kabi, Anbieter von Gesundheitsprodukten für kritisch und chronisch Kranke, gehört Fresenius Helios zum Gesundheitskonzern Fresenius. Mit seinen rund 130.000 Mitarbeitenden der Helios Gruppe in Deutschland sowie Quirónsalud in Spanien und Lateinamerika erzielte Fresenius Helios 2025 einen Gesamtumsatz von mehr als 13,5 Milliarden Euro.
Quirónsalud verfügt über 57 Kliniken, davon sieben in Lateinamerika, rund 130 ambulante Gesundheitszentren sowie über 300 Einrichtungen für betriebliches Gesundheitsmanagement. Jährlich werden hier rund 22 Millionen Patient:innen behandelt, davon mehr als 20 Millionen ambulant. Quirónsalud beschäftigt rund 50.000 Mitarbeitende und erwirtschaftete 2025 einen Umsatz von mehr als 5,4 Milliarden Euro.
leben / 20.05.2026
Frühlingskonzert und Ehrung für Professor Heinz Bielka

Der Freundeskreis des Max Delbrück Center lud zum klassischen Konzert auf dem Campus ein und eröffnete anschließend eine neue Galerie für Ehrenplaketten von CAMPUSart
Junge, musikalisch hochbegabte Musikerinnen und Musiker haben, unterstützt durch ihre Lehrerin, die Klavierprofessorin Prof. Galina Iwanzowa-Bielka, am 13. Mai ein weiteres Mal bei einem Konzert auf dem Campus ihr breites Repertoire klassischer Musik dargeboten. Die meisten der jungen Talente sind bereits Preisträger verschiedener internationaler Wettbewerbe.
Schon seit mehr als einem Jahrzehnt verfolgen wir die Entwicklung von Schülerinnen und Schülern der beliebten Pianistin aus Buch. Wir sehen ihnen beim Großwerden zu und bestaunen ihre musikalische Entwicklung über die vielen Jahre, vom schüchternen Kind, das mit seinen kleinen Händen schon beachtlich über die Klaviertasten wirbelt, bis zu den jungen Erwachsenen, die von Jahr zu Jahr virtuoser geworden sind. Man ist gerührt und voller Begeisterung. Da der Kirchturm inzwischen fertiggestellt ist, der über die Jahre das Spendenanliegen von Prof. Heinz Bielka und seiner Frau Prof. Galina Iwanzowa war, gehen die Spenden der treuen Zuhörerschaft dieses Mal an das Ronald McDonald Haus am Helios Klinikum in Buch, zugunsten von Familien schwerkranker Kinder. Ein Teil davon soll weitere Veranstaltungen des MDC-Freundeskreises finanzieren.
Im Anschluss an das Konzert sind die Besucher ein paar Schritte um das Haus herumgegangen, um gemeinsam mit dem Freundeskreis die erste Ehrenplakette in der geplanten Galerie für Wissenschafts-Persönlichkeiten zu enthüllen, die sich für den Campus Berlin-Buch, für Medizin und Wissenschaft sowie für unseren Stadtteil verdient gemacht haben.
Die Galerie wurde am Walter-Friedrich-Haus (Haus 27), nahe dem Eingangsbereich mit der Freitreppe, eröffnet. Die erste Ehrenplakette ist Herrn Prof. Dr. Heinz Bielka (1929-2020) gewidmet. Professor Bielka hat von 1953 bis zu seinem Tode auf dem Campus Buch als Krebsforscher gearbeitet und sich als Chronist des Campus, von Berlin-Buch sowie durch seinen beständigen Einsatz für den Stadtteil, darunter für die Wiedererrichtung des Kirchturms der Schlosskirche, große Verdienste erworben.
Die hier entstehende Galerie ist Teil des Projektes „CAMPUSart“, das verschiedene Rundgänge zur Wissenschaftsgeschichte, zur Botanik oder auch zu Skulpturen anbietet sowie auch Ausstellungen, wie zu der Künstlerin Jeanne Mammen, eine Mikroskopausstellung und das Campusmuseum. Broschüren für diese Rundgänge findet man im Café Max im Torhaus, und auch wochentags zu den Arbeitszeiten im Infozentrum des Gläsernen Labors auf dem Campus. Alle Exponate, die im Rahmen von CAMPUSart zu sehen sind, auch die neue Plakette, sind mit einem QR-Code versehen, der dann ausführliche Informationen dazu auf das Smartphone gibt, sodass man den Rundgang oder einen einfachen Spaziergang jederzeit auch allein starten kann.
Text: Michaela Langer
Quelle: Bucher Bote
CAMPUSart
heilen, bilden / 20.05.2026
Einladung zum Tag der offenen Tür - „Room of Horror“ statt Langeweile
Wer glaubt, Gesundheitsberufe bestünden nur aus Teetrinken und Händchenhalten, sollte sich am 18. Juni warm anziehen. Die Akademie der Gesundheit e.V. öffnet am Campus Berlin-Buch ihre Tore und zeigt, dass Ausbildung auch „Room of Horror“, OP-Action und High-Tech-Simulation bedeuten kann.
Was macht eigentlich eine ATA im OP, außer cool auszusehen? Wie fühlt es sich an, mit 80 Jahren durch einen Parkour zu navigieren? Und wer gewinnt die Reanimations-Challenge? Antworten auf diese Fragen gibt es am 18. Juni 2026 von 11:00 bis 17:00 Uhr live vor Ort.
Erleben. Ausprobieren. (Vielleicht auch kurz Gruseln.)
Die Akademie, die seit 30 Jahren Profis für den Gesundheitsmarkt schmiedet, gewährt am Tag der offenen Tür einen exklusiven Blick in den Maschinenraum der modernen Ausbildung. An über 20 Mitmach-Stationen können Besucher selbst Hand anlegen:
• Chirurgie für Anfänger: Am Laparoskopie-Trainer echtes OP-Feeling schnuppern.
• Der „Room of Horror“: Pflegesimulation mal ganz anders – Fehler finden, bevor es brenzlig wird.
• Teddy-Klinik: Für die Kleinsten (und alle, die ihren Kuschelbären verarzten wollen).
• Check-up: Blutdruck- und Blutzuckermessungen für alle, die wissen wollen, ob der Power-Level noch im grünen Bereich ist.
Karrierekick inklusive
Für alle, die nicht nur zum Gucken kommen, stehen unsere Bildungsberater bereit. Ob Pflegefachkraft, Physiotherapie oder die spannenden medizinisch-technischen Berufe – wir zeigen, wie Ausbildung heute funktioniert: modern, interaktiv und garantiert ohne Staubschicht.
Der Eintritt ist frei – die Neugier ist Pflicht!
Wann: 18. Juni 2026, 11:00 – 17:00 Uhr (Schulklassen bereits ab 11:00 Uhr)
Wo: Akademie der Gesundheit e.V., Campus Berlin-Buch, Schwanebecker Chaussee 4 E-H, 13125 Berlin
leben / 19.05.2026
Baumaßnahmen an der Park-and-Ride-Anlage Pankow-Heinersdorf abgeschlossen
Die Park-and-Ride-Anlage (P+R) am Bahnhof Pankow-Heinersdorf ist nach umfangreichen Neubau- und Sanierungsmaßnahmen wieder vollständig nutzbar. Das Straßen- und Grünflächenamt Pankow hat die Arbeiten mit einem Investitionsvolumen von rund 550.000 Euro Ende April 2026 abgeschlossen. Finanziert wurde das Projekt mit Unterstützung der Senatsverwaltung für Mobilität, Verkehr, Klimaschutz und Umwelt.
Im Rahmen der Maßnahme wurden zahlreiche schadhafte Bereiche der Parkflächen sowie angrenzende Gehwege grundlegend saniert. Der Neubau des Gehwegs entlang der Pasewalker Straße sowie einer neuen Gehwegvorstreckung in der Straße Am Feuchten Winkel erhöhen nicht nur die Attraktivität zur Nutzung der Park-and-Ride-Anlage, sondern tragen auch maßgeblich zur Steigerung der Verkehrssicherheit bei.
Auch die Beschilderung der Anlage wurde umfassend erneuert und optimiert. Sie erleichtert Kraftfahrern die Orientierung bei der Anfahrt zu den Stellflächen und bietet zugleich ein übersichtliches Leitsystem für Fußgänger durch eine gezielte Wegweisung zu den Zugängen des S-Bahnhofs. Dabei wird gezielt auf die Differenzierung der Barrierefreiheit der unterschiedlichen Zugänge (Treppe oder Aufzug) geachtet.
Darüber hinaus wurden die Stellplätze unterhalb der Autobahnbrücke markiert. Dadurch wird der ruhende Verkehr besser geordnet, die vorhandenen Flächen können effizienter genutzt und ungewollte Wendemanöver reduziert werden.
Ute Bonde, Senatorin für Mobilität, Verkehr, Klimaschutz und Umwelt:
„Moderne Mobilität braucht starke Verknüpfungspunkte. Mit der Sanierung der Park-and-Ride-Anlage in Pankow-Heinersdorf schaffen wir bessere Bedingungen für alle, die flexibel zwischen Auto, S-Bahn und Fußverkehr wechseln. Die Investition stärkt nicht nur die Verkehrssicherheit und Barrierefreiheit vor Ort, sondern ist auch ein weiterer Schritt hin zu einem vernetzten, klimafreundlichen und alltagstauglichen Mobilitätssystem für Berlin.“
Manuela Anders-Granitzki, Bezirksstadträtin für Ordnung und Öffentlicher Raum:
„Mit der Sanierung der Park-and-Ride-Anlage verbessern wir nicht nur die Verkehrssicherheit vor Ort, sondern stärken auch die Verknüpfung verschiedener Mobilitätsangebote im Bezirk. Die neue Wegeführung, die auf Barrierefreiheit ausgerichtete Beschilderung und die bessere Ordnung der Stellflächen machen die Anlage für die Nutzer deutlich attraktiver und sicherer.“
Die P+R-Anlage Pankow-Heinersdorf ist ein zentraler Knotenpunkt für Pendler und Besucher. Die nun abgeschlossenen Arbeiten unterstreichen das Engagement von Bezirksamt und Senatsverwaltung für eine zukunftsfähige Verkehrsinfrastruktur.
leben / 18.05.2026
Pankow macht sich Klimafit! Online-Beteiligung bis 14. Juni und 2. Öffentliche Werkstatt am 4. Juni
Das Bezirksamt Pankow lädt zur weiteren Mitwirkung an der Erarbeitung des bezirklichen Klimaanpassungskonzepts (KLAK) ein.
Der Klimawandel ist auch in Pankow deutlich spürbar: Immer häufiger gibt es extreme Hitze im Sommer, lange Trockenzeiten und Starkregen. Diese Entwicklungen stellen den Bezirk und die Bürgerinnen und Bürger vor Herausforderungen. Mit dem Klimaanpassungskonzept (KLAK) sollen konkrete Lösungen entwickelt werden, um Pankow Schritt für Schritt besser auf diese Folgen vorzubereiten. Ziel ist es, grünere, kühlere und widerstandsfähige Stadträume zu schaffen und die Aufenthaltsqualität zu verbessern.
Ein wichtiger Teil des Konzepts ist die Öffentlichkeitsbeteiligung. In der ersten Phase Ende 2025 brachten die Beteiligten ihre Erfahrungen mit Hitze und Starkregen sowie Ideen und Hinweise zur Klimaanpassung ein. Jetzt geht die Beteiligung in die zweite Phase. Im Mittelpunkt stehen Maßnahmen, die das Stadt- und Quartiersklima verbessern, für Abkühlung sorgen und vor Überschwemmungen durch Starkregen schützen. Auch in der aktuellen Phase ist eine Beteiligung sowohl bei einer Präsenzveranstaltung als auch digital möglich:
2. Öffentliche Werkstatt am 4. Juni
Wann? Do., 04. Juni 2026, 16:00 – 18:00 Uhr
Wo? Ökomarkt am Kollwitzplatz, Wörther Straße, 10435 Berlin
Das Bezirksamt präsentiert sich mit einem Mitmach-Stand auf dem Ökomarkt am 04.06.2026. Dort können sich Interessierte über die bisherigen Ergebnisse informieren und konkrete Maßnahmenvorschläge kennenlernen. Interessierte können abstimmen, welche Vorschläge Sie für besonders wichtig halten und eigene Ideen einbringen. Alle sind herzlich eingeladen, vorbeizukommen und sich zu beteiligen.
2. Online-Beteiligung vom 18. Mai bis 14. Juni
Zusätzlich besteht die Möglichkeit, vom 18. Mai - 14. Juni 2026 an der Online-Beteiligung teilzunehmen um Maßnahmenvorschläge zu verorten und zu priorisieren:
https://mein.berlin.de/projekte/klimaanpassungskonzept-pankow/
Das Klimaanpassungskonzept wird durch ein interdisziplinäres Team des Büros gruppe F | Freiraum für alle GmbH im Auftrag des Bezirksamtes Pankow erarbeitet.
Weitere Informationen gibt es auf der Seite des Umwelt- und Naturschutzamtes:
Mit freundlichen Grüßen,
Ulrike Plüschke
Bezirksamt Pankow von Berlin
Pressestelle
Rathaus Pankow
Breite Str. 24A-26
13187 Berlin
Raum 1.01
Tel.: 030 - 90 295 2211
E-Mail: ulrike.plueschke@ba-pankow.berlin.de
Schon abonniert? https://www.berlin.de/pankow-news
produzieren / 12.05.2026
Eckert & Ziegler mit erfolgreichem Jahresauftakt. Prognose 2026 bestätigt.
1. Quartal 2026:
- Umsatz 72,9 Mio. € (VJ: 68,2 Mio. €)
- EBIT vor Sondereinflüssen 16,0 Mio. € (VJ:16,2 Mio. €)
- Nettogewinn 10,4 Mio. € (VJ: 9,7 Mio. €)
Jahresprognose 2026:
- Umsatz von rund 320 Mio. € (bestätigt)
- EBIT vor Sondereinflüssen von rund 80 Mio. € (bestätigt)
Die Eckert & Ziegler SE (ISIN DE0005659700, TecDAX) konnte ihren Umsatz im ersten Quartal 2026 im Vergleich zum Vorjahreszeitraum um 7% auf 72,9 Mio. € steigern. Aufgrund eines etwas schwächeren Produktmix im Segment Isotope Products in den ersten zwei Monaten des Jahres sank das bereinigte Konzern-EBIT um 2% auf 16,0 Mio. €. Der Nettogewinn erhöhte sich um 7% auf 10,4 Mio. € oder 0,17€ pro Aktie.
Die Umsätze im Segment Medical lagen in den ersten drei Monaten des Jahres mit 41,5 Mio. € deutlich über dem Niveau des Vorjahres (34,4 Mio. €). Nach wie vor bleibt das Geschäft mit pharmazeutischen Radioisotopen der wichtigste Umsatzbringer. Dabei sind insbesondere die Entwicklung der Umsätze mit Generatoren und im Bereich Contract Manufacturing & Development (CDMO) zu nennen.
Das Segment Isotope Products erzielte mit 31,5 Mio. € einen um 2,3 Mio. € oder etwa 7% niedrigeren Umsatz als in den ersten drei Monaten des Vorjahres. Auf ein starkes viertes Quartal 2025, folgte ein verhaltener Start in das Jahr, welches im März wieder deutlich an Dynamik gewann.
Die am 26. März 2026 veröffentlichte Prognose für das Geschäftsjahr 2026 bleibt unverändert. Der Vorstand rechnet weiterhin mit einem Umsatz von rund 320 Mio. € und einem bereinigtem EBIT von rund 80 Mio. €.
Den vollständigen Quartalsbericht finden Sie hier: https://www.ezag.com/Q12026de
Über Eckert & Ziegler.
Die Eckert & Ziegler SE gehört mit über 1.000 Mitarbeitern zu den führenden Anbietern von isotopentechnischen Komponenten für Nuklearmedizin und Strahlentherapie. Das Unternehmen bietet weltweit an seinen Standorten Dienstleistungen und Produkte im Bereich der Radiopharmazie an, von der frühen Entwicklung bis hin zur Kommerzialisierung. Die Eckert & Ziegler Aktie (ISIN DE0005659700) ist im TecDAX der Deutschen Börse gelistet.
Wir helfen zu heilen.
leben, bilden / 06.05.2026
Kleine Partikel ganz groß

Die Thementage „Unsichtbare Welten“ im Zeiss Großplanetarium nahmen im April Mikroplastik in den Fokus. Mit dabei: das Max Delbrück Center und das Gläserne Labor
Zum zweiten Mal veranstaltete die Stiftung Planetarium Berlin im Zeiss Großplanetarium die Thementage Unsichtbare Welten. Statt wie sonst mit Teleskopen in den Weltraum zu blicken, erkundeten die Besucher und Besucherinnen bei dieser Veranstaltung mit Mikroskopen den Mikrokosmos. Mit dabei war wieder der Campus Buch, mit Experimentierstationen im Foyer und Live-Beiträgen im Kuppelsaal.
Plastik im Kopf?
Wir leben in einer Plastikwelt. Kein Lebensbereich kommt ohne Kunststoffe aus, zu zahlreich die Vorteile, zu vielseitig die über 16.000 Varianten. Doch nicht alles wird recycelt, ein Großteil landet in der Natur. Statt zu verrotten, wird Plastik mit der Zeit in immer kleinere Fragmente zerrieben, zerrissen und zerbrochen. Aus Makro- wird Mikroplastik. Doch es bleibt Plastik. Die winzigen Teilchen lassen sich überall finden, Untersuchungen zufolge auch in unseren Körpern. Was tun sie da? Beeinflussen die winzigen Partikel Mensch und Natur? Wenn ja, wie?
International arbeiten viele Institutionen mit Hochdruck daran, diesen drängenden Fragen zu beantworten. So wird am Max Delbrück Center erforscht, ob mikroskopische Kunststoffteile in menschliche Gehirnzellen eindringen können und was sie dort bewirken. Im Rahmen der Berlin Brains Vortragsreihe präsentierten sechs Forschende des Max Delbrück Center, Paula Leupold, Georg Braune, Ivanna Kupryianchyk-Schulz, Robert Zinzen, Yi-Ming Zhang und Florian Bartsch, ihre Arbeit im Kuppelsaal des Planetariums in aufwendigen 360° Fulldome Visualisierungen. Ihr Beitrag zeigte: Zellen können unter Laborbedingungen Partikel aufnehmen und verpacken sie in kleine Bläschen. Gesundheitliche Schäden konnten bislang nicht festgestellt werden, doch die Forschung steht noch am Anfang.
Komm und sieh selbst
Andere Fragen konnten sich Gäste unter Anleitung selbst beantworten: Wie können Plastikarten getrennt werden und wo lassen sich die mikroskopischen Fragmente finden? Das Team des MINT-Schülerlabors des Campus Buch half, vorbereitete und selbst mitgebrachte Proben professionell zu untersuchen. Die Experimentierstationen des Gläsernen Labors wurden über die drei Tage begeistert von Jung und Alt genutzt.
Dabei wurden auch Präparate für eine weitere Veranstaltung im Kuppelsaal erstellt. Bei der "Mega-Mikroskopie" führte die Leiterin des Gläsernen Labors, Claudia Jacob, gemeinsam mit dem Initiator der Veranstaltung, Jochen Müller, das Publikum in die Welt der Kunststoffe durch alle Größenordnungen, von Makro bis Nano. Als ein Highlight der Thementage mikroskopierte Jochen Müller live an zwei von Zeiss zur Verfügung gestellten Mikroskopen, wobei das Bild eindrucksvoll in die Kuppel projiziert wurde.
Gleich ob Einzelpersonen, Familien oder Schulklassen, das Interesse war groß, auch die eigenen Objekte gemeinsam auf der größten Leinwand Berlins zu bestaunen oder zu erkennen, was dort vergrößert dargestellt wurde.
Mit ihren interaktiven Angeboten konnten die teilnehmenden Einrichtungen beim Publikum das Bewusstsein für die jetzt schon offenkundigen Folgen von Mikroplastik oder die möglichen Risiken in Mensch und Natur schärfen. Neben dem Gläsernen Labors waren dies: das Freilandlabor Marzahn, die Berliner Mikroskopische Gesellschaft, die deutsche Meeresstiftung und das Bundeinstitut für Risikobewertung.
Text: Dr. Jochen Müller für die buchinside 2/26
forschen, produzieren, heilen, bilden / 22.04.2026
Erster gemeinsamer Career Day vernetzt Wissenschaft und Wirtschaft

Der Career Day des Max Delbrück Center bot jungen Forschenden in Kooperation mit dem Betreiber des Campus Berlin-Buch Einblicke in die Arbeitswelt von Start-ups und Biotechs
Der 16. April war ein dicht gepackter Tag für die Teilnehmenden des Career Days des Max Delbrück Centers mit dem Titel „Transition possible – Explore Careers Beyound R&D“. Zahlreiche Doktoranden und Postdocs erhielten Einblicke in mögliche Karrieren außerhalb der akademischen Welt.
Eröffnet wurde die Veranstaltung vom Biologen Lars Dittrich, der als Wissenschaftsredakteur bei MaiThink X arbeitet. Am Vormittag gab es Helmholtz-übergreifend virtuelle Vorträge zu Karrierewegen außerhalb der Forschung. Die Referenten stellten konkrete Einstiegs- und Entwicklungsmöglichkeiten und teilten ihre Erfahrungen zum Wechsel aus der Wissenschaft in andere Berufsfelder.
Am Nachmittag hatten das Max Delbrück Center und die Campus Berlin-Buch GmbH ins Gründerzentrum BerlinBioCube eingeladen. Hier stellten sich die Berlin BioScience Academy und das Innovation & Entrepreneurship Department des Max Delbrück Center vor. Anschließend gab es Laborführungen in Biotech-Unternehmen und einen Workshop zum Bewerbungsprozess.
Wege in die Biotech- und Pharmabranche
Wie erhält man fundierte Einblicke in die Biotech- und Pharmabranche, ohne Teil davon zu sein? Die Berlin BioScience Academy (BBA) bietet genau diese Möglichkeit. In ihren Kursen vermittelt sie biotechnologische und pharmakologische Prozesse bis hin zu Good Manufacturing Practise (GMP) oder Good Clinical Practise (GCP). „Wer einen Wechsel in die Industrie erwägt oder den Sprung in ein Start-up wagen möchte, erhält in der Biotech & Pharma Summer School in kürzester Zeit einen Überblick über den gesamten Prozess der Arzneimittelentwicklung, von der Idee bis zum Markt“, sagte Dr. Uwe Lohmeier, der die BBA leitet. Im Eventformat „Talk im Cube“ vernetzt die BBA regelmäßig Wissenschaft und Wirtschaft und bietet Panel-Diskussionen zu Themen wie Finanzierungsstrategien, Female Founders, CRO oder IP Strategies in Biotechnology. Auch hier bietet sich unkompliziert die Gelegenheit, mit Biotechfirmen ins Gespräch zu kommen.
Am Max Delbrück Center bietet die Abteilung Innovation & Entrepreneurship ein Sprungbrett für eine Karriere in Spin-offs. Dr. Nevine Shalaby, zeigte Fördermöglichkeiten für künftige „Sciencepreneurs“ auf, um innovative Diagnostik- oder Therapieansätze für die Anwendung zu entwickeln. Das Innovation-Office unterstützt unter anderem mit Programmen wie BOOST und PreGoBio, um Ideen und deren grundsätzliche Umsetzbarkeit zu validieren, hilft Finanzierungen einzuwerben, bietet Mentoring, stellt Kontakte zu Industrie und Investoren her und begleitet die Geschäftsentwicklung proaktiv.
Wie arbeiten Biotech-Unternehmen?
Über 50 Biotech- und Medtech-Unternehmen haben sich im BiotechPark Berlin-Buch angesiedelt, darunter zahlreiche Start-ups. Vier davon öffneten am Career Day ihre Türen, vermittelten den Teilnehmenden, wie sie arbeiten und welches ihre Mission ist. Mit T-knife, Spin-off von Max Delbrück Center und Charité, stellte sich ein junges, biopharmazeutisches Unternehmen vor, das T-Zell-Therapien der nächsten Generation zur Bekämpfung von Krebs entwickelt.
CheckImmune, Spin-off der Charité, informierte über seine Arbeit als akkreditiertes Speziallabor, das u.a. mit immunologischen Studien die klinische Entwicklung neuer Therapeutika begleitet.
In den Laboren von Biosynth erfuhren die Teilnehmenden, mit welchen Technologien polymerbasierte Hilfsstoffe für die Arzneimittelabgabe sowie Biokonjugat-Arzneimittel entwickelt und hergestellt werden. Nicht zuletzt präsentierte das Team von FyoniBio sein Spektrum an Auftragsentwicklung und klinischen Laborleistungen.
„Es sind überraschend viele verschiedene Firmen vor Ort“, so eine Teilnehmerin, die sich gut vorstellen könnte, in einer der Biotechfirmen zu arbeiten: „Die Labore im BioCube ähneln denen der Forschungseinrichtungen, und das Gebäude wirkt sehr großzügig, gerade auch durch die großen gemeinsamen Teeküchen.“ Einer der Teilnehmenden hob positiv überrascht hervor, wie divers die Alterspanne der Beschäftigten in Start-ups sein kann. Spannend war für viele zu erfahren, wie die Arbeitskultur in einem Start-up funktioniert, und dass dort andere, vielfältigere Tätigkeiten als in der reinen Wissenschaft anstehen.
Wie erfolgreich ist meine Bewerbung?
In einem gemeinsamen Workshop bot der Career Day zum Abschluss die Möglichkeit, in die Rolle einer Personalverantwortlichen zu schlüpfen. Anita Überheim, Head of Human Resources Europe der weltweit agierenden Eckert & Ziegler SE, ließ die Teilnehmenden drei anonymisierte CV und Bewerbungsanschreiben beurteilen und erläuterte anschließend, welche Aspekte bei der Auswahl zählen. Sie beschrieb, wie Personaler vorgehen, wieviel Zeit bleibt, die Bewerbungen zu erfassen, welche Skills zu nennen wichtig und welche Fehler typisch sind. Schließlich führte die Expertin mit einer Teilnehmenden ein kurzes Probevorstellungsgespräch. Bei der gemeinsamen Auswertung mit dem Publikum erläuterte sie, wie die Bewerbenden am besten kommunizieren und reagieren sollten. Neben vielen hilfreichen Tipps war eine zentrale Erkenntnis für die Nachwuchstalente: Es müssen nicht immer 90 Prozent von den gewünschten Qualifikationen erfüllt sein. Viel wichtiger sei, dass die Person ins Team passt und sich mit ihrem Potenzial noch entwickeln kann.
Der gemeinsame Career Day fand großen Anklang. „Wir freuen uns, dass wir diesen Tag mitgestalten konnten. Der Career Day gibt ganz konkrete Einblicke in die Biotechbranche und vernetzt junge Talente mit potenziellen Arbeitgebern am Standort, das ist für alle Beteiligten wertvoll“, sagt Dr. Ulrich Scheller, Geschäftsführender der Campus Berlin-Buch GmbH.
www.campusberlinbuch.deforschen, heilen / 17.04.2026
Grundlegend neuer Therapieansatz gegen Mukoviszidose: Nanobody repariert Zelldefekt
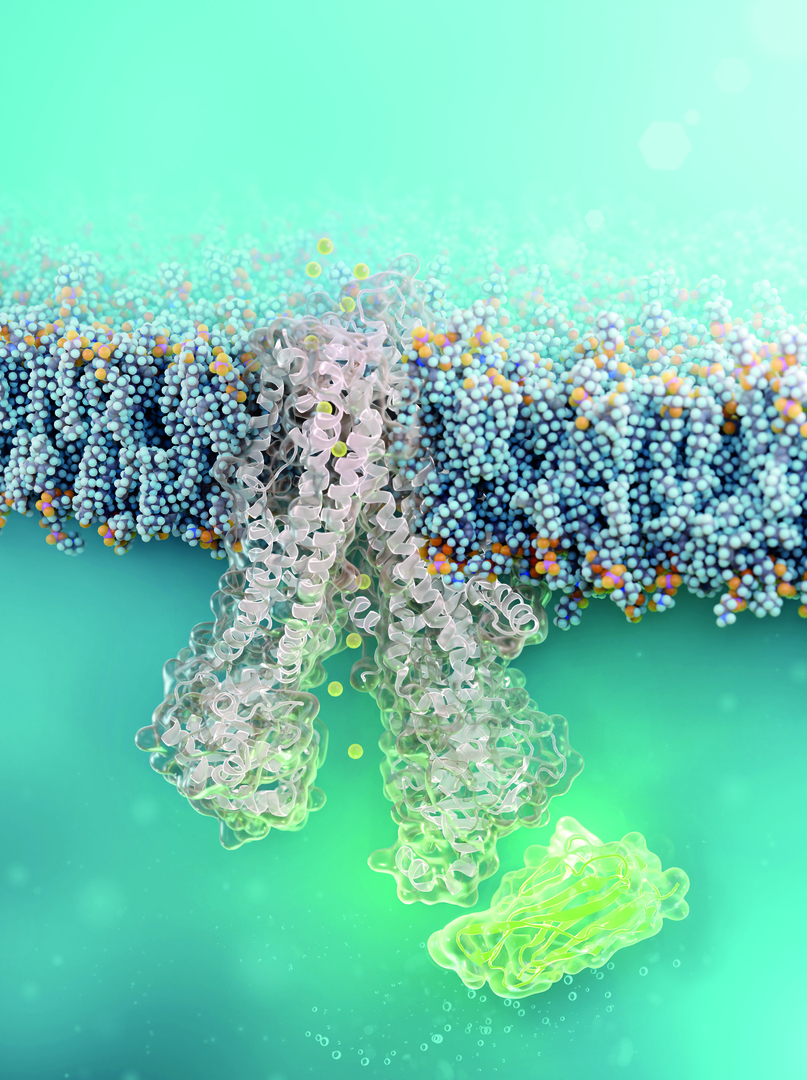
Ein winziger Antikörperbaustein könnte die Behandlung von Mukoviszidose grundlegend verändern: Forschenden ist es erstmal gelungen, einen sogenannten Nanobody zu entwickeln, der direkt in menschliche Zellen eindringt und den am häufigsten fehlerhaften Chloridkanal bei Mukoviszidose reparieren kann. Der neue Therapieansatz wurde gemeinsam von Teams des Leibniz-Forschungsinstituts für Molekulare Pharmakologie (FMP) und der Charité – Universitätsmedizin Berlin entwickelt. Erstautor:innen der Studie, die kürzlich im renommierten Fachmagazin Nature Chemical Biology veröffentlicht wurde, sind Luise Franz (FMP) und Tihomir Rubil (Charité).
Das Krankheitsbild der Mukoviszidose – auch Cystische Fibrose (kurz CF) genannt – beruht auf Gendefekten im sogenannten CFTR-Kanal. Er reguliert den Wasser- und Salztransport in der Lungenschleimhaut und sorgt für die Bildung ausreichend flüssigen Schleims. Bei etwa 90 Prozent der Mukoviszidose-Patient:innen liegt eine als F580del bezeichnete Mutation im CFTR-Kanal vor, das heißt, in seiner Proteinkette fehlt an Position 508 eine einzelne Aminosäure. Diese Veränderung führt dazu, dass CFTR falsch gefaltet und im Inneren der Zelle vorzeitig abgebaut wird, statt als Kanal in der Zellmembran der Atemwege zu arbeiten. Betroffene haben dadurch zähen Schleim in der Lunge, Erreger können nicht mehr gut abtransportiert werden. Die Folge ist eine chronische Infektion und Entzündung der Atemwege, die zu einem fortschreitenden Verlust der Lungenfunktion führt – im schlimmsten Fall macht das eine Lungentransplantation nötig.
Prof. Marcus Mall, Direktor der Klinik für Pädiatrie mit Schwerpunkt Pneumologie, Immunologie und Intensivmedizin an der Charité, hat mit seinem Team in den letzten Jahren maßgeblich dazu beigetragen, die Behandlung von Mukoviszidose durch eine Therapie mit drei niedermolekularen Wirkstoffen (CFTR-Modulatoren) spürbar zu verbessern: Mithilfe der Dreifachtherapie aus Elexacaftor, Tezacaftor und Ivacaftor (ETI) kann die Funktionsweise des CFTR-Kanals auf etwa 50 Prozent des normalen Werts angehoben werden. Die chronische Entzündung und Infektion der Lunge bestehen aber häufig fort, zudem gibt es Patient:innen, bei denen diese Therapie nicht wirkt oder die sie nicht vertragen.
Ein Antikörper als Reparaturhelfer
Für diese Gruppe könnte es künftig weitere Behandlungsoptionen geben: Das Team um den Chemiker Prof. Christian Hackenberger vom Leibniz-FMP hat im Labor ein neues Molekül entwickelt, das das fehlgefaltete CFTR direkt im Zellinneren stabilisiert. Hierbei handelt es sich um einen Nanobody – ein winziger, aber stabiler Antikörperbaustein, der sich präzise an definierte Oberflächen von Proteinen anlagern kann. Dieser wird chemisch mit einem „Transportsignal“, sogenannten zellpenetrierenden Peptiden, versehen, die ihm helfen, direkt in Schleimhautzellen der Lunge einzudringen. Dort bindet der Nanobody an das defekte Kanal-Protein und hilft ihm, die richtige Form anzunehmen.
Die Forschenden konnten zeigen, dass sich der Nanobody in Zellen, die von Mukoviszidose-Patient:innen stammten, über mindestens 24 Stunden an den mutierten CFTR-Kanal heftete. Die Zellen schädigte er dabei nicht. Funktionelle Untersuchungen belegten zudem, dass der korrigierte Kanal wieder Chlorid über die Zellmembran transportierte.
Kombination aus Dreifachtherapie und Nanobody
In Kombination mit der etablierten ETI-Dreifachtherapie zeigte der Nanobody in diesen Zellkulturen einen ausgeprägten Synergieeffekt: Während die ETI-Wirkstoffe die Funktion des defekten CFTR-Kanals im Mittel etwa zur Hälfte wiederherstellten, ließ sich die Kanal-Aktivität durch die zusätzliche Gabe des Nanobodys auf knapp 90 Prozent des Normalniveaus steigern.
Damit zeigt die Studie, dass von außen zugegebene zellgängige Nanobodys krankheitsrelevante, fehlgefaltete Proteine im Inneren von Zellen stabilisieren und ihre Funktion wiederherstellen können. „Es handelt sich, neben dem präklinischen Machbarkeitsnachweis einer Reparatur des CFTR-Kanals, um das erste Beispiel eines funktionalen zellpermeablen Antikörpers: Bisher wurden zellgängige Nanobodys vor allem zum Sichtbarmachen intrazellulärer Zielstrukturen oder zur gezielten Abtötung von Zellen eingesetzt“, sagt Christian Hackenberger.
„Da die Nanobodys direkt im Bereich der F508del-Mutation binden, ermöglichen sie es, die Reifungsstörung der CFTR-Kanäle noch gezielter zu behandeln“, sagt Marcus Mall. „Durch diesen neuen Wirkmechanismus lässt sich die CFTR-Funktion in Kombination mit den bestehenden CFTR-Modulatoren deutlich besser korrigieren. Unsere Ergebnisse deuten darauf hin, dass mit diesem neuen Ansatz sogar eine vollständige Normalisierung der CFTR-Funktion möglich ist. Dies wäre ein weiterer Durchbruch für die Therapie der Mukoviszidose.“ Die Arbeit eröffnet neue Möglichkeiten, die Behandlung von Mukoviszidose weiter zu verbessern – und legt zugleich den Grundstein für breitere therapeutische Anwendungen.
Perspektiven über Mukoviszidose hinaus
Bis zu einer klinischen Anwendung des Ansatzes bei Mukoviszidose müssen jedoch noch zentrale Fragen gelöst werden, etwa eine geeignete Formulierung für eine inhalative Anwendung und eine effiziente Durchdringung des zähen CF-Schleims. Zudem ist noch unklar, wie der Nanobody im Körper wirkt und wie das Immunsystem auf eine Nanobody-Behandlung reagiert. Diese Herausforderungen werden aktuell im Sonderforschungsbereich 1449 „Dynamische Hydrogele an Biogrenzflächen“ bearbeitet, in dessen Rahmen auch die aktuellen Ergebnisse entstanden sind.
Der Ansatz einer intrazellulären Nanobody-Therapie könnte auch über Mukoviszidose hinaus bei anderen seltenen genetischen Krankheiten hilfreich sein, bei denen Proteinfehlfaltung eine Rolle spielt und für die es bisher kaum wirksame Behandlungen gibt.
Über Mukoviszidose
Mukoviszidose oder Cystische Fibrose ist eine der häufigsten tödlich verlaufenden Erbkrankheiten weltweit. In Deutschland sind bis zu 8.000 Kinder, Jugendliche und Erwachsene davon betroffen. Durch eine Störung des Salz- und Wasserhaushalts im Körper bildet sich bei Mukoviszidose-Betroffenen ein zähflüssiges Sekret, das Organe wie die Lunge und die Bauchspeicheldrüse schädigt. Das führt zu einem fortschreitenden Verlust der Lungenfunktion und Atemnot, was die Lebenserwartung trotz verbesserter Behandlungsansätze noch immer deutlich senkt. Jedes Jahr werden in Deutschland etwa 150 bis 200 Kinder mit der seltenen Krankheit geboren. Ein Test auf Mukoviszidose ist Teil des Neugeborenen-Screenings.
Quelle: Gemeinsame Pressemitteilung von Charité und FMP
Grundlegend neuer Therapieansatz gegen Mukoviszidose: Nanobody repariert Zelldefekt
bilden / 15.04.2026
Von gesunder Ernährung bis zur Funktionsweise der Sinne

Das Gläserne Labor bietet 2026 in Kooperation mit der Grundschule Am Sandhaus erneut die Forscher-AG FIN an. Ermöglicht wird dies durch das Deutsche Zentrum für Kinder- und Jugendgesundheit
Die Arbeitsgemeinschaft (AG) „FiN – Fit in den Naturwissenschaften“ möchte Fünft- und Sechstklässler der Bucher Grundschule Am Sandhaus für naturwissenschaftliche Fragestellungen begeistern und ihre experimentellen Kompetenzen entwickeln. Themenschwerpunkt ist die Gesundheit von Heranwachsenden. In diesem Jahr wird die AG durch das Deutsche Zentrum für Kinder- und Jugendgesundheit (DZKJ) gefördert.
Im ersten Teil der AG erfahren die Kinder, wie Ernährung auf die Gesundheit wirkt. Sie beschäftigen sich mit gesunder Ernährung, ermitteln mit Labormethoden den Zuckergehalt von Lebensmitteln und setzen sich mit der Volkskrankheit Diabetes auseinander. Die AG wirkt auch in den Alltag hinein, denn die Kinder führen eine Woche gemeinsam mit ihrer Familie ein Ernährungstagebuch. Bei der Auswertung geht es darum zu vermitteln, wie eine ausgewogene Ernährung aussehen sollte und wie viele positive Effekte diese haben kann. Zum Abschluss wird gemeinsam gekocht – gesund und lecker.
Danach beschäftigt sich die AG mit dem Nervensystem und den Sinnen. Experimente vermitteln anschaulich die Funktionsweise der Nerven, ihr Zusammenspiel und die Bedeutung der Sinne für die Wahrnehmung. Wie ist das Gehirn aufgebaut, wie funktionieren die Augen und das Gehör? Für gesunde Menschen sind diese Fähigkeiten selbstverständlich, doch welche Einschränkungen ergeben sich bei neurologischen Erkrankungen? Dies testen die Kinder anschaulich mittels einer Prismenbrille beim Ballspielen.
„Wir freuen uns sehr, dass wir die AG bereits im zweiten Jahr bei uns im Schülerlabor anbieten können. Es ist eine ganz praktische Heranführung an eine bewusstere Wahrnehmung der Gesundheit, die zugleich erklärt, was Erkrankungen auslösen kann – und wie wichtig Prävention ist“, sagt Biologin Claudia Jacob, die die AG im Gläsernen Labor leitet.
Informationen zu Arbeitsgemeinschaften im Gläsernen Labor
News auf der Webseite des Gläsernen Labors
Von gesunder Ernährung bis zur Funktionsweise der Sinne
produzieren / 14.04.2026
Eckert & Ziegler: Metzler nimmt Research Coverage mit Kauf-Empfehlung und einem Kursziel von 21,00 € auf. Kurspotenzial 41%
B. Metzler seel. Sohn & Co. AG (Bankhaus Metzler) hat die Research Coverage der Eckert & Ziegler SE (ISIN DE0005659700) einem führenden Anbieter von isotopentechnischen Komponenten für Nuklearmedizin und Messtechnik, mit Kauf-Empfehlung und einem Kursziel von 21,00 € aufgenommen. Dies entspricht einem Kurspotenzial von 40,8 % gegenüber dem Xetra-Schlusskurs von 14,92 € am 13. April 2026.
Das Bankhaus Metzler hebt damit die starke Marktpositionierung der Eckert & Ziegler SE hervor, die von der steigenden Nachfrage nach diagnostischen und therapeutischen Radioisotopen in der Nuklearmedizin profitiert.
Über Eckert & Ziegler.
Die Eckert & Ziegler SE gehört mit über 1.000 Mitarbeitern zu den führenden Anbietern von isotopentechnischen Komponenten für Nuklearmedizin und Strahlentherapie. Das Unternehmen bietet weltweit an seinen Standorten Dienstleistungen und Produkte im Bereich der Radiopharmazie an, von der frühen Entwicklung bis hin zur Kommerzialisierung. Die Eckert & Ziegler Aktie (ISIN DE0005659700) ist im TecDAX der Deutschen Börse gelistet.
Quelle: Pressemitteilung Eckert & Ziegler SE
Eckert & Ziegler SE
forschen, heilen / 13.04.2026
Erste Proteinkarte von schmerzauslösenden Neuronen
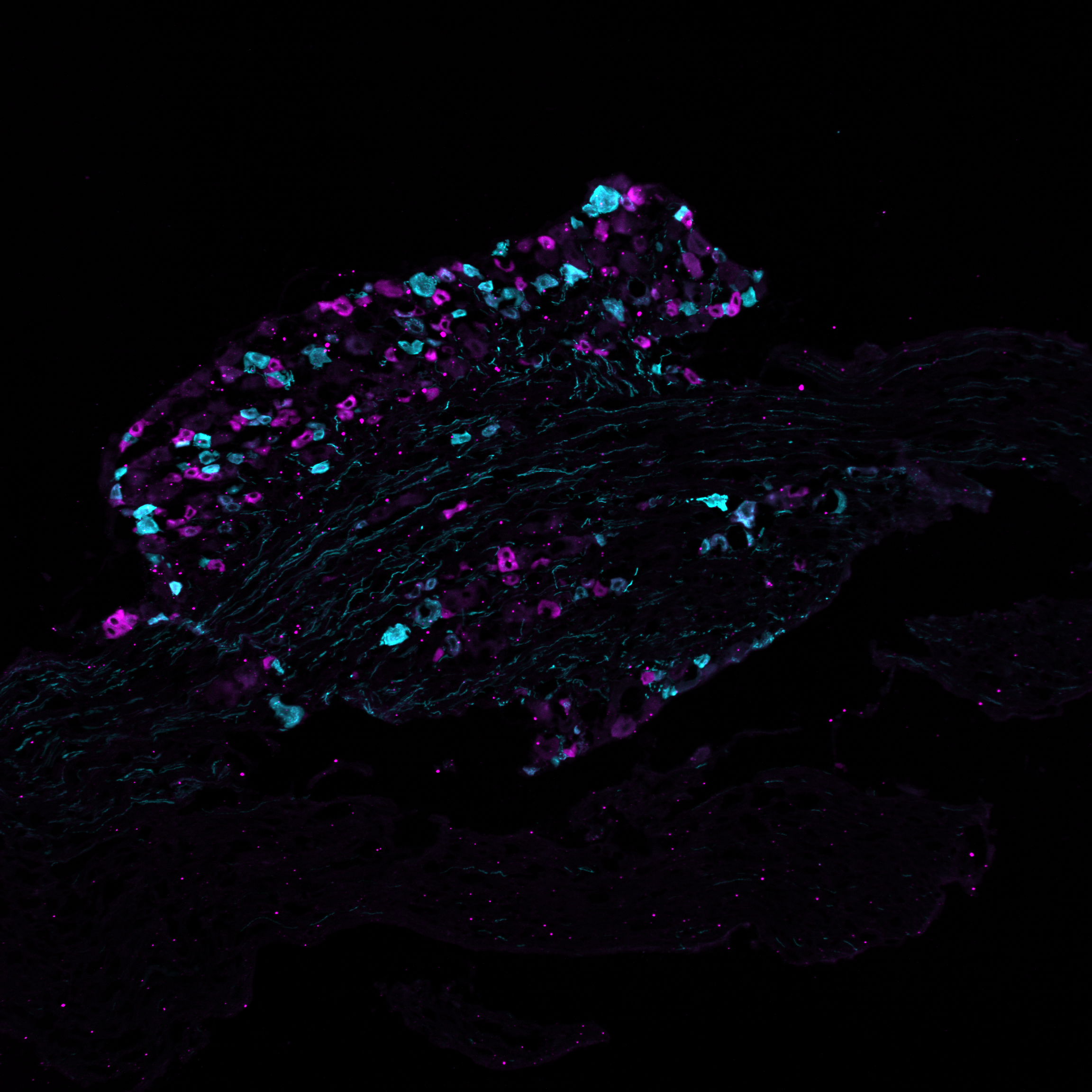
Helmholtz-Forschende haben die erste detaillierte Proteinkarte von Schmerzneuronen erstellt. Ihre in „Nature Communications“ veröffentlichte Studie hilft, die molekularen Mechanismen chronisch-entzündlicher Schmerzen besser zu verstehen und neue Zielstrukturen für Medikamente zu finden.
Jeder fünfte Mensch weltweit leidet an chronisch-entzündlichen Schmerzen. Bisher erhältliche Schmerzmittel können diese bei zwei Dritteln der Betroffenen kaum lindern. Völlig neue Ansätze für Medikamente werden daher dringend benötigt. „Um sie entwickeln zu können, müssen wir erst einmal genau verstehen, wie die sensorischen Nervenzellen den Schmerz auf molekularer Ebene auslösen – welche Proteine also daran beteiligt sind“, sagt Professor Gary Lewin, der Leiter der Arbeitsgruppe „Molekulare Physiologie der somatosensorischen Wahrnehmung“ am Berliner Max Delbrück Center.
Um diese molekularen Prozesse zu entschlüsseln, arbeitet Lewin – der sich seit vier Jahrzehnten mit dem Thema Schmerz beschäftigt und erst kürzlich einen bis dahin unbekannten Ionenkanal entdeckt hat, der an der Schmerzwahrnehmung beteiligt ist – eng mit dem Systembiologen Dr. Fabian Coscia zusammen. Coscia leitet am Max Delbrück Center die Arbeitsgruppe „Spatial Proteomics“ und hat die Methode Deep Visual Proteomics mitentwickelt. Mit diesem Verfahren lässt sich das Proteom – also die Gesamtheit aller Proteine – spezifisch für einzelne Zelltypen und räumlich aufgelöst bestimmen.
Die Forschenden kombinierten diese Technologie mit elektrophysiologischen Methoden aus Lewins Arbeitsgruppe. Dadurch konnten sie spezifische Subtypen von Schmerzneuronen zunächst funktionell identifizieren und anschließend ihre Proteinprofile analysieren. So entstand eine hochauflösende molekulare Karte dieser Nervenzellen, die die beiden Wissenschaftler jetzt gemeinsam mit ihren Kolleg*innen im Fachblatt „Nature Communications“ vorgestellt haben. Zudem erläutern die Forschenden, wie sich mit ihrem Ansatz potenzielle neue Wirkstoffziele finden lassen, um chronische Schmerzen zu behandeln.
Erstautorin der Studie ist Dr. Sampurna Chakrabarti. Die Forscherin war Postdoc in Lewins Team und leitet inzwischen ihre eigene Arbeitsgruppe „Mechanismen der Infektion und Nozizeption“ am Helmholtz-Zentrum für Infektionsforschung (HZI) in Braunschweig. Nozizeption ist der Fachbegriff für die Wahrnehmung von Schmerzen; die beteiligten Nervenzellen bezeichnet man als Nozizeptoren. Sie enden in schmerzempfindlichen Geweben des Körpers, zum Beispiel in der Haut, den Muskeln und Gelenken. Dort nehmen sie schmerzauslösende Signale wahr, die sie ans Gehirn weiterleiten.
Bislang unentdeckte Signalwege
Nicht alle Nozizeptoren sind gleich. „Bis jetzt waren von verschiedenen Subtypen lediglich die Transkriptome bekannt, also Informationen zur RNA“, sagt Chakrabarti. „Die eigentlichen Funktionsträger aller Zellen sind aber die Proteine, die anhand der RNA-Abschriften gebildet werden – sie haben wir uns jetzt in zwei Subtypen von Nozizeptoren erstmals genauer angeschaut.“ Mithilfe einer elektrophysiologischen Methode, der Patch-Clamp-Technik, hat das Team in Spinalganglien von Mäusen die beiden Subtypen, die als peptiderg und nicht-peptiderg bezeichnet werden und Schmerzen von unterschiedlicher Art und Dauer auslösen können, zunächst aufgespürt und genauer charakterisiert.
Um eine spezifische Proteinkarte von beiden Zelltypen zu erstellen, verwendeten die Forschenden jeweils etwa 50 solcher Neuronen. Deep Visual Proteomics kombiniert Massenspektrometrie mit Mikroskopie, künstlicher Intelligenz und Robotik. Coscia und sein Team haben die Methodik bislang vor allem für Proteomanalysen von Krebszellen genutzt. „Jetzt konnten wir erstmals zeigen, dass sich das Verfahren auch auf Nervenzellen anwenden lässt“, sagt der Forscher.
Mehr als 6.000 Proteine haben er und seine Kolleg*innen in diesen 50 Neuronen jeweils messen können. Ein Vergleich mit vorhandenen RNA-Daten zeigte, dass sich das Transkriptom und das Proteom der Zellen teilweise deutlich voneinander unterscheiden – ein Hinweis darauf, dass wichtige funktionelle Prozesse erst auf Proteinebene sichtbar werden. „Mit dieser Studie liefern wir eine bislang einzigartige molekulare Karte von schmerzauslösenden Neuronen“, sagt Coscia. „Sie ermöglicht es, in den Zellen Signalwege zu identifizieren, die bisher verborgen geblieben sind.“
Im nächsten Schritt der Studie wollten Chakrabarti und ihre Kolleg*innen verstehen, durch welche Proteine Nervenzellen sensibler werden und so zu chronischen Schmerzen beitragen. Dazu isolierten sie aus den Spinalganglien der Mäuse beide Subtypen der Nozizeptoren und setzten die Zellen in der Kulturschale über Nacht dem Nervenwachstumsfaktor NGF (Nerve Growth Factor) aus. Von ihm ist bekannt, dass er an der Entstehung chronischer Schmerzen auch beim Menschen, zum Beispiel bei Arthritis, beteiligt ist. Mithilfe von Deep Visual Proteomics konnten die Forschenden im Anschluss die Proteine, die die Zellen in Anwesenheit von NGF produziert hatten, präzise identifizieren.
Weniger empfindlich gegen Schmerzsignale
Dass NGF bei chronisch-entzündlichen Schmerzen eine wichtige Rolle spielt, entdeckte Lewin gemeinsam mit seinem Team schon vor mehr als 30 Jahren. „Bei Hunden und Katzen lassen sich Schmerzen mit Antikörpern, die NGF hemmen, mittlerweile sehr gut lindern“, sagt Lewin. „Beim Menschen haben seltene Nebenwirkungen ihren Einsatz leider verhindert“, ergänzt der Forscher. „Jetzt aber haben wir womöglich einen alternativen Weg gefunden: Er zielt auf ein nachgeschaltetes Protein ab, das für die sensibilisierende Wirkung von NGF verantwortlich ist.“
„Wir haben mehrere Proteine identifiziert, die nach der Behandlung mit NGF in einem Subtyp der Nozizeptoren vermehrt vorkamen. Die erhöhten Konzentrationen dieser Proteine könnten mit chronisch-entzündlichen Schmerzen in Verbindung stehen“, berichtet Chakrabarti. Eines der Proteine, ein Enzym namens B3GNT2, stach besonders hervor. „Wenn wir in den Zellen das dazugehörige Gen ausschalteten, ließ die entzündungsbedingte Hyperaktivität der Nozizeptoren nach“, sagt die Forscherin: „Auf einen leichten mechanischen Reiz reagierten dann weniger Zellen als zuvor.“ Mit anderen Worten: Die Neuronen wurden unempfindlicher – und würden so im Körper deutlich weniger Schmerzen auslösen.
Als Nächstes wollen die Forschenden ihre Ergebnisse, die sie mit isolierten Zellen erzielt haben, an Mäusen und menschlichen Zellen überprüfen. „Mehr als 90 Prozent aller zugelassenen Medikamente zielen mittlerweile auf Proteine ab“, sagt Coscia. „Das zeigt, wie wichtig es ist, ein besseres Verständnis für diese Moleküle zu entwickeln, um neue Zielstrukturen für effektivere Schmerzmittel und Wirkstoffe gegen andere neurologische Erkrankungen zu entdecken.“
Foto: Schnitt durch ein Spinalganglion einer Maus, in dem zwei unterschiedliche Typen von Schmerzrezeptoren in Cyan (türkis) und Magenta (pink) angefärbt sind. © Sampurna Chakrabarti, Max Delbrück Center
Gemeinsame Pressemitteilung des Max Delbrück Center und des Helmholtz-Zentrums für Infektionsforschung
Weitere Informationen:
Lewin Lab
Molecular Physiology of Somatic Sensation
Coscia Lab
Spatial Proteomics
- AG Chakrabarti
- Porträt Gary Lewin
- Porträt Fabian Coscia
- Proteinlandkarten von Tumoren
- Die Wurzeln chronischer Schmerzen verstehen
Literatur: Sampurna Chakrabarti, Anuar Makhmut, Atena Mohammadi et al. (2026): „Deep visual proteomics uncovers nociceptor diversity and pain targets“. Nature Communications, DOI:10.1038/s41467-026-71418-8
produzieren / 10.04.2026
Eckert & Ziegler sichert Zugang zu entscheidender Augentumorbehandlung durch MDR-Zertifizierung für Ru-106 Augenapplikatoren
Eckert & Ziegler BEBIG GmbH, eine Tochter der Eckert & Ziegler SE mit Fokus auf Brachytherapie-Lösungen für die Behandlung von Augentumoren sowie Prostatakrebs, hat von den zuständigen Behörden die MDR-Zertifizierung für ihre Ruthenium-106 (Ru-106) Augenapplikatoren erhalten. Eckert & Ziegler ist der einzige globale Anbieter dieser Augenapplikatoren. Daher ist dieser wichtige Meilenstein eine kritische Absicherung gegen Versorgungsengpässe.
Die Medical Device Regulation (MDR) ist eine Verordnung der Europäischen Union (EU 2017/745) mit dem Ziel, die Qualität von Medizinprodukten zu verbessern und die Patientensicherheit zu erhöhen. Die Zertifizierung garantiert die langfristige Verfügbarkeit der Ru-106 Augenapplikatoren innerhalb der EU. Dieses Medizinprodukt wird von Eckert & Ziegler bereits seit über 30 Jahren hergestellt und international angeboten. Es wird aktiv in fast 50 Ländern eingesetzt und steuert jährlich mehrere Millionen Euro Umsatz zum Ergebnis der Eckert & Ziegler Gruppe bei.
Bei der ophthalmologischen Brachytherapie wird eine kleine radioaktive Platte, welche Ru-106 enthält, genutzt, um Aderhautmelanome bei Erwachsenen oder Retinoblastome bei Kindern zu behandeln. Die Platte wird an die Augenwand in unmittelbarer Nähe zum Tumor aufgenäht. Dort verbleibt sie für mehrere Tage, bis die notwendige Strahlung abgegeben wurde. Als Alternative zur Entfernung des betroffenen Auges, bietet diese Behandlungsmethode den Patient:innen eine Chance zum Erhalt von Sehkraft und Lebensqualität.
"Der Einsatz unseres Teams für die MDR-Zertifizierung eines Nischenproduktes wie dem Ru-106 Augenapplikator demonstriert unser Engagement dafür, Patient:innen und Behandlungszentren langfristig mit dieser wichtigen Therapieform versorgen zu können", erklärte Katrin Antonenko, Geschäftsführerin der Eckert & Ziegler BEBIG GmbH. "Dieser Meilenstein steht zudem für den anhaltenden Verdienst des Produktes, das vor über drei Jahrzehnten den Weg für das nachhaltige und erfolgreiche Wachstum der Eckert & Ziegler Gruppe ebnete. Die Erfahrung aus der erfolgreichen Zulassung wird uns beim Vorantreiben weiterer Projekte zugutekommen."
Über Eckert & Ziegler
Die Eckert & Ziegler SE gehört mit über 1.000 Mitarbeitern zu den führenden Anbietern von isotopentechnischen Komponenten für Nuklearmedizin und Strahlentherapie. Das Unternehmen bietet weltweit an seinen Standorten Dienstleistungen und Produkte im Bereich der Radiopharmazie an, von der frühen Entwicklung bis hin zur Kommerzialisierung. Die Eckert & Ziegler Aktie (ISIN DE0005659700) ist im TecDAX der Deutschen Börse gelistet.
Quelle: Pressemitteilung Eckert & Ziegler SE
Eckert & Ziegler sichert Zugang zu entscheidender Augentumorbehandlung durch MDR-Zertifizierung für Ru-106 Augenapplikatoren
forschen / 08.04.2026
Gilead übernimmt FMP- und LMU-Spin-off Tubulis und erweitert Onkologie-Pipeline um ADC der nächsten Generation
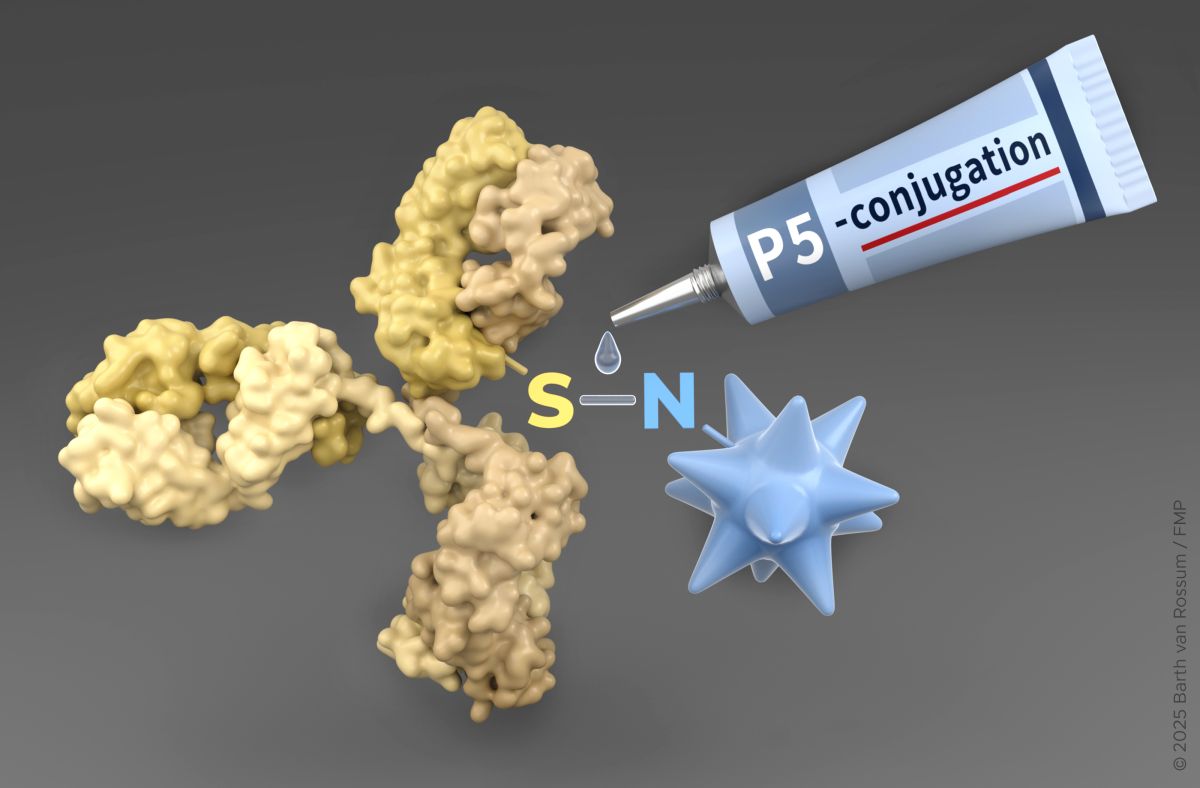
Das US-amerikanische Biopharmaunternehmen Gilead hat eine endgültige Vereinbarung zur Übernahme der Tubulis GmbH geschlossen. Tubulis wurde 2019 aus dem Leibniz-Forschungsinstitut für Molekulare Pharmakologie (FMP) und der LMU München ausgegründet und entwickelt Antikörper-Wirkstoff-Konjugate (ADCs) der nächsten Generation, die darauf ausgelegt sind, verschiedene Wirkstoffe selektiver an Tumore abzugeben und den Nutzen für die Patient:innen zu maximieren. Mit der Transaktion wird die Onkologie Pipeline von Gilead um mehrere innovative Programme und Plattformtechnologien erweitert, deren Ursprung teilweise in der akademischen Forschung des Leibniz Forschungsinstituts für Molekulare Pharmakologie (FMP) in Berlin liegt.
Die Übernahme umfasst das führende Produkt von Tubulis, TUB‑040, ein gegen NaPi2b gerichtetes Topoisomerase‑I‑Inhibitor‑ADC, das sich derzeit in Phase-1b/2 der klinischen Entwicklung zur Behandlung von platinresistentem Eierstockkrebs und nicht‑kleinzelligem Lungenkrebs (NSCLC) befindet. Gilead wird zudem TUB‑030 übernehmen, ein gegen 5T4 gerichtetes ADC mit vielversprechenden frühen klinischen Daten bei verschiedenen soliden Tumorarten sowie die ADC-Plattform der nächsten Generation von Tubulis und eine vielversprechende frühe Pipeline.
Dr. Dominik Schumacher, CEO und Mitgründer von Tubulis, betont die Bedeutung der Kombination aus wissenschaftlicher Exzellenz und industrieller Entwicklungsstärke: „Von Anfang an waren wir davon überzeugt, dass unsere Konjugationstechnologieplattformen weitreichende Auswirkungen auf den gesamten ADC-Bereich haben könnten, und die ersten Daten zu TUB-040 haben diese Überzeugung bestärkt“, sagt Dr. Dominik Schumacher, Chief Executive Officer und Mitbegründer von Tubulis. „Der Beitritt zu Gilead ermöglicht es uns, auf dieser Grundlage innerhalb einer Organisation aufzubauen, die über fundiertes wissenschaftliches Fachwissen, globale Entwicklungskapazitäten und die erforderliche Größe verfügt, um Innovationen in Medikamente für Patienten und Patientinnen weltweit umzusetzen. Durch unsere bestehende Zusammenarbeit hat Gilead bereits das Potenzial unserer Technologien erkannt, und gemeinsam sind wir gut aufgestellt, um die Entwicklung unserer ADC-Pipeline zu beschleunigen. Ich bin dem Tubulis-Team, unserem Vorstand, unseren Investoren und Partnern zutiefst dankbar für ihr Engagement und dafür, dass sie dazu beigetragen haben, diesen Meilenstein zu erreichen.“
P5-Konjugationstechnologie vom FMP
Eine Schlüsselrolle in der Produktentwicklung von Tubulis spielt die innovative P5‑Konjugationstechnologie, eine Linkerchemie, die die präzise Verknüpfung von Antikörpern mit hochpotenten Wirkstoffen ermöglicht. Entwickelt wurde sie in der Grundlagenforschung von Prof. Dr. Christian Hackenberger, einem der Mitgründer von Tubulis, und seinem Team am Leibniz‑Forschungsinstitut für Molekulare Pharmakologie (FMP). Tubulis hat die P5‑Technologie in Kooperation mit der Arbeitsgruppe von Prof. Dr. Heinrich Leonhardt (Ludwig-Maximilians-Universität München), einem Mitbegründer von Tubulis, für die klinische Forschung und Anwendung weiterentwickelt. "Diese erfolgreiche Technologieentwicklung zeigt das Potential interdisziplinärer Kooperationen über Fakultäts- und Institutsgrenzen hinweg", sagt Prof. Dr. Heinrich Leonhardt. Diese Technologie bildet heute eine zentrale Plattform für die stabile und kontrollierte Wirkstoffabgabe in den ADC‑Programmen des Unternehmens. „Diese Übernahme unterstreicht nicht nur den Erfolg unserer Konjugationstechnologie und die Leistung des Tubulis Teams mit neuen ADCs die Krebstherapie zu verbessern. Sie zeigt auch wie wichtig die Grundlagenforschung an Universitäten und Forschungsinstituten für die translationale Innovation ist“, sagt Prof. Dr Christian Hackenberger.
Nach Abschluss der Transaktion wird Tubulis als eigenständige ADC‑Forschungsorganisation innerhalb von Gilead agieren, wobei der Standort München als Drehscheibe für ADC-Innovationen dienen wird. Dabei wird auf bestehende integrierte Kompetenzen in Forschung, Produktion und klinischer Entwicklung aufgebaut, um ADCs der nächsten Generation voranzutreiben.
Gilead wird das gesamte ausstehende Eigenkapital von Tubulis für eine Barzahlung in Höhe von 3,15 Milliarden US‑Dollar auf einer „cash-free, debt-free“-Basis sowie für bis zu 1,85 Milliarden US‑Dollar an erfolgsabhängigen Meilensteinzahlungen erwerben. Der Abschluss der Übernahme wird für das zweite Quartal 2026 erwartet. Der Abschluss der Transaktion steht unter dem Vorbehalt des Ablaufs oder der Aufhebung bestimmter behördlichen Genehmigungen sowie weiterer üblicher Abschlussbedingungen.
Über Tubulis
Tubulis entwickelt maßgeschneiderte Antikörper-Wirkstoff-Konjugate (ADCs) mit verbesserten biophysikalischen Eigenschaften. In präklinischen Modellen haben die ADCs bereits eine gezielte und dauerhafte Anreicherung im Tumor sowie langanhaltende Anti-Tumor-Wirkungen gezeigt. Die beiden am weitesten fortgeschrittenen Programme in der wachsenden Pipeline sind TUB-040 (gerichtet gegen NaPi2b) und TUB-030 (gerichtet gegen 5T4). Beide Programme werden derzeit in klinischen Studien bei Krebserkrankungen mit einem hohen medizinischen Bedarf untersucht. Weitere Informationen unter: www.tubulis.com
Quelle: Leibniz-Forschungsinstitut für Molekulare Pharmakologie
Gilead übernimmt FMP- und LMU-Spin-off Tubulis und erweitert Onkologie-Pipeline um ADC der nächsten Generation
leben / 31.03.2026
Spaziergänge im Pankower Norden mit Cordelia Koch: erste Tour startet am 11. April in Blankenburg
Die Bezirksbürgermeisterin Cordelia Koch lädt gemeinsam mit Wanderleiter Eckehard Heiber vom Sportverein Empor-Berlin alle Interessierten ein, den Pankower Norden bei vier Wanderung im April, Juni, August und September zu Fuß zu entdecken.
Der Bezirk hat mit der Entwicklung eines Freiraum- und Erholungskonzeptes die Grundlage für ein gutes Miteinander von Natur, Erholung, Tourismus und Gewerbe verabschiedet. Um die einzelnen Entwicklungsstufen und -regionen vorzustellen, werden an vier Samstagen in diesem Frühjahr und Sommer je eine Wanderung angeboten. Die Spaziergänge stehen jeweils unter einem Motto. Begleitet wird die Bezirksbürgermeisterin von Eckehard Heiber, der passionierter und erfahrener Wanderleiter sowie Initiator des jährlichen Wanderplanes für den SV-Empor-Berlin ist. Er wird entlang des Weges auf die Besonderheiten der Natur, auf die Stadtentwicklung im Kontext zur Geschichte als auch auf die architektonischen Kleinode hinweisen. Die Bezirksbürgermeisterin ergänzt mit Informationen aus dem Freiraum- und Erholungskonzept sowie zu politischen Themen entlang der Route. Cordelia Koch: „Zwischen Autobahn und Bahntrasse – einfach schön? Der Pankower Norden bietet reizvolle Wanderwege, die zu Spaziergängen abseits der Großstadt einladen.“
Wanderung am 11. April für von Blankenburg nach Weißensee
Die erste Wanderung steht unter dem Motto „Marder, Mörder, Gärtner oder Künstler“ und findet am Samstag, dem 11. April 2026 von 09:30 bis 12:30 Uhr statt. Treffpunkt ist auf dem Vorplatz des S-Bahnhofs Blankenburg. Die ca. acht Kilometer lange Route verläuft entlang der Anlage Blankenburg, des Mörderbergs zur Stadtrandsiedlung Malchow über den Sportkomplex Rennbahnstraße bis zur Kunsthalle am Hamburger Platz in Weißensee.
Weitere Termine:
· 20.06.2026: Entdeckungen in der Schönholzer Heide und in Wilhelmsruh
· 08.08.2026: „Ein Zipfel von Berlin“ – Wanderung in Buch
· 12.09.2026: „Von Mönchmühle nach Blankenfelde”
Die Wanderrungen finden jeweils von 9:30 bis 12:30 statt und sind auch für ältere oder nicht trainierte Menschen geeignet.
Anmeldung erforderlich
Wegen der begrenzten Zahl der Teilnehmenden wird um Anmeldung gebeten: per E-Mail an buergermeisterin@ba-pankow.berlin.de oder per Telefon: +49 30 90295-2301. Die Teilnahme an den Wanderungen kostenlos. Spenden zu Gunsten des Kinderhospizes Sonnenhof der Björn-Schulz-Stiftung werden gern entgegengenommen.
Weitere Informationen: https://www.berlin.de/ba-pankow/spaziergaenge
leben / 27.03.2026
Siegerentwurf für das Neue Stadtquartier Elisabeth-Aue

Das im November 2025 gestartete kooperative Werkstattverfahren für das Neue Stadtquartier Elisabeth-Aue ist am 26. März 2026 erfolgreich abgeschlossen worden. Die Jury hat aus vier Entwürfen den städtebaulichen Entwurf von Hosoya Schaefer Architects AG mit AgenceTer.de GmbH Landschaftsarchitekten ausgewählt, der bildet die Grundlage für die weiteren Planungsschritte.
Auf der rund 73 ha großen landeseigenen Fläche der Elisabeth-Aue soll ein gemischtes, ökologisches und nachhaltiges Stadtquartier der kurzen Wege entstehen. Geplant sind 5.000 neue Wohnungen sowie ergänzend Dienstleistungen, Einzelhandel, Büros, Schulen sowie weitere soziale und kulturelle Einrichtungen. Um einen qualifizierten städtebaulichen und freiraumplanerischen Entwurf für die Entwicklung des Neuen Stadtquartiers zu erarbeiten, wurde ein städtebaulich-freiraumplanerischer Realisierungswettbewerb nach RPW durchgeführt. Der anonyme Wettbewerb wurde gemeinsam von der Senatsverwaltung für Stadtentwicklung, Bauen und Wohnen und der Entwicklungsgesellschaft Elisabeth-Aue GmbH ausgelobt. Zwölf Planungsteams aus Deutschland und Europa haben sich beteiligt. Unter dem Vorsitz von Herr Prof. Kunibert Wachten bewertete das Preisgericht die zwölf eingereichten Wettbewerbsarbeiten und prämierte vier Entwürfe, die weiter vertieft werden sollen.
In der anschließenden kooperativen Werkstatt ab November 2025 wurden die vier Entwürfe basierend auf den Hinweisen der Jury und der Öffentlichkeit weiterentwickelt und konkretisiert.
Die Arbeiten wurden abschließend von der Jury vergleichend bewertet. Man hat sich für den Entwurf des Büros Hosoya Schaefer Architects AG mit AgenceTer.de GmbH Landschaftsarchitekten entschieden (siehe Lageplan und Fußgängerperspektive). Dieses Konzept zeigt besonders überzeugende Antworten zu den vielfältigen Anforderungen des Standorts auf und zeichnet sich durch eine hohe städtebauliche Qualität aus. Der Entwurf überzeugt durch vier grüne Anger-Kieze, die mit einem großzügigen Park verbunden sind. Damit wird im neuen Stadtquartier eine hohe Wohnqualität geschaffen.
Neben dem ausgewählten Entwurf, gab es weitere Entwürfe, die durch die Jury gewürdigt wurden.
Sie haben wertvolle Impulse für die Entwicklung des Standorts geliefert. Die Entwürfe sind von folgenden Teams erstellt worden:
- CITYFÖRSTER architecture+urbanism PartGmbB, arbos landscape GmbH, ARGUS Stadt und Verkehr Partnerschaft mbB
- Ortner & Ortner Baukunst Gesellschaft von Architekten mbH, capattistaubach urbane landschaften Landschaftsarchitekt und Architekten PartGmbH
- 03 Arch. GmbH, Kuehn Malvezzi Projects GmbH, ver.de Landschaftsarchitekten Stadtplaner Partnerschaftsgesellschaft mbB
Prof. Petra Kahlfeldt, Senatsbaudirektorin und Staatssekretärin für Stadtentwicklung:
„Ich freue mich sehr, dass mit dem ausgewählten Entwurf eine überzeugende Grundlage für die weitere Entwicklung der Elisabeth-Aue vorliegt. Der Siegerentwurf überzeugt mit einem qualitativ hochwertigen städtebaulichen und landschaftsplanerischen Konzept und meistert die planerischen Herausforderungen des Neuen Stadtquartiers. Das mehrstufige Verfahren hat besonders qualitätsvolle Beiträge hervorgebracht und es hat mir gezeigt, welches Potenzial in der Elisabeth-Aue liegt.“
Prof. Dipl-Ing. Kunibert Wachten, Vorsitzender der Jury:
„Alle vier Entwürfe haben sich intensiv mit der anspruchsvollen Aufgabenstellung auseinandergesetzt und individuell überzeugende städtebauliche und freiraumplanerische Lösungen für diese besondere Lage am Stadtrand entwickelt. Mit dem ausgewählten Siegerentwurf verfügen die Auslobenden nun über eine gestalterisch qualitativ hochwertige und technisch wie wirtschaftlich belastbare Grundlage für die nächsten Schritte in der Planung eines zukunftsweisenden Stadtquartiers.“
Kathrin Drogosch, Geschäftsführerin Entwicklungsgesellschaft Elisabeth-Aue GmbH:
„Mit dem ausgewählten Siegerentwurf liegt eine hervorragende Grundlage für die Realisierung von nachhaltigem und bezahlbarem Wohnraum vor. Es entsteht ein gemischtes, grünes und innovatives Stadtquartier eingebettet in eine besondere landschaftliche Kulisse.“
Öffentliche Veranstaltung und Präsentation des Siegerentwurfs
Zur Abschlussveranstaltung und Präsentation des Siegerentwurfs am 14.04.2026 ist die Öffentlichkeit herzlich eingeladen. In der Veranstaltung wird das Planungsteam den Siegerentwurf vorstellen. Zudem wird ein Ausblick auf die weiteren Schritte im Planungsprozess gegeben. Fragen und Anregungen aus der Stadtgesellschaft sind ausdrücklich erwünscht.
Wann: 14.04.2026, 18:00-20:30 Uhr (Einlass ab 17:00 Uhr)
Wo: SchuleEins, Berliner Straße 120, 13187 Berlin (Eingang über Hadlichstraße)
Die Veranstaltung ist kosten- und barrierefrei. Wegen begrenzter Plätze kann der Einlass kann nur mit Anmeldung garantiert werden: https://eveeno.com/elisabethaue.
forschen / 27.03.2026
Friedrich-Stolz-Preis für das Tubulis-Team

Die Fachgruppe Medizinische Chemie der Gesellschaft Deutscher Chemiker (GDCh) und die Fachgruppe Pharmazeutische/Medizinische Chemie der Deutschen Pharmazeutischen Gesellschaft (DPhG) haben den Friedrich-Stolz-Preis 2026 an das Team von Tubulis verliehen – einem Spin-off des Leibniz-Forschungsinstituts für Molekulare Pharmakologie (Leibniz-FMP) und der LMU München. Ausgezeichnet wurden Prof. Dr. Christian Hackenberger vom Leibniz-FMP als Mitgründer und Berater sowie Dr. Jonas Helma-Smets, Mitgründer und CSO, Dr. Marc-André Kasper, VP Chemistry and Early Discovery, und Dr. Annette Vogl, VP Biology and Translational Research, von Tubulis.
Der Friedrich-Stolz-Preis würdigt außergewöhnliches Engagement, wissenschaftliche Entdeckungen oder innovative Technologien mit nachgewiesener Relevanz, die zu substanziellen therapeutischen Innovationen oder nachhaltigen Entwicklungen beitragen und über frühe Forschungsphasen hinausgehen.
Das Tubulis-Team wurde für seine P5-Ethynylphosphonamidat-Konjugationschemie ausgezeichnet, die einen neuartigen Typ von Antikörper-Wirkstoff-Konjugaten (ADCs) ermöglicht. Die Konjugationschemie, auch als P5-Labeling bezeichnet, wurde am FMP in der Forschungsgruppe von Christian Hackenberger entwickelt. Diese neue ADC-Klasse zeichnet sich durch außergewöhnliche Plasma-Stabilität, günstige pharmakokinetische Eigenschaften und starke anti-tumorale Wirksamkeit aus. Darauf aufbauend wurden NaPi2b-bindende Exatecan-ADCs mit besonders stabilen Linkern, reduzierter Off-Target-Toxizität und optimierter molekularer Architektur entwickelt. Höhepunkt dieser Arbeit ist der Entwicklungskandidat TUB-040, der in einer klinischen Phase-1-Studie bei Patientinnen mit platinresistentem Ovarialkarzinom vielversprechende Tumorremissionen, eine breite therapeutische Breite und gute Verträglichkeit zeigt. Damit demonstriert die Forschung, wie innovative Chemie direkt in neuartige, potenziell wirksamere Behandlungsoptionen für schwer behandelbare Krebsarten übersetzt werden kann.
Der Preis wird im Gedenken an den Industrieapotheker und Arzneimittelforscher Friedrich Stolz verliehen, dessen visionäre Innovationskraft als Vorbild für anwendungsorientierte, therapeutisch relevante Forschung dient.
Foto: Auszeichnung mit dem Friedrich-Stolz-Preis 2026: Prof. Dr. Stefan Laufer (GDCh), Prof. Dr. Christian Hackenberger, Dr. Annette Vogl, Dr. Jonas Helma-Smets, Dr. Franz von Nussbaum (von links). © GDCh
Quelle: Mitteilung FMP
Friedrich-Stolz-Preis für das Tubulis-Team
produzieren / 26.03.2026
Eckert & Ziegler: Erfolgreiches Geschäftsjahr 2025 mit positivem Ausblick
Die Eckert & Ziegler SE (ISIN DE0005659700, TecDAX) erreichte im Geschäftsjahr 2025 mit einem Umsatz von 312,0 Mio. € eine neue Rekordmarke. Im Vergleich zum Vorjahr stieg der Umsatz um rund 16 Mio. € (+5%). Das EBIT vor Sondereinflüssen aus fortgeführten Geschäftsbereichen (bereinigtes EBIT) legte gegenüber dem Vorjahr um knapp 12 Mio. € auf 77,7 Mio. € zu (+18%). Der Jahresüberschuss stieg um rund 15 Mio. € (+46%) auf 48,8 Mio €; dies entspricht einem Ergebnis pro Aktie von 0,78 € (Vj. splitbereinigt 0,53 €).
Im Segment Medical erhöhte sich der Umsatz um 22,6 Mio. € oder 15% auf 171,3 Mio. €. Nach wie vor bleibt das Geschäft mit pharmazeutischen Radioisotopen der wichtigste Umsatzbringer.
Das Segment Isotope Products erzielte mit 150,1 Mio. € einen um 7,9 Mio. € (-5%) gesunkenen Umsatz gegenüber dem Vorjahr. Grund hierfür sind im Vergleich zum Vorjahreszeitraum temporäre Verschiebungen hin zu margenschwächeren Produkten. Darüber hinaus führte die Cyberattacke in 2025 zu projektbezogenen Verzögerungen.
Für das Geschäftsjahr 2026 rechnet der Vorstand mit einem bereinigten EBIT von rund 80 Mio. €. Die dazugehörige Umsatzerwartung beläuft sich auf rund 320 Mio. €. Voraussetzungen für die Prognose ist ein gewichteter Durchschnittskurs von 1,20 USD pro Euro. Bereinigt um Wechselkurseffekte und das Lizenzgeschäft entspräche dies einem Wachstum von 9% im Umsatz und 21% im Ergebnis (bereinigtes EBIT).
Vorstand und Aufsichtsrat werden der Hauptversammlung eine Dividende in Höhe von 0,22 € (Vj. splitbereinigt 0,17 €) je dividendenberechtigter Aktie vorschlagen.
Den vollständigen Jahresabschluss 2025 finden Sie hier: https://www.ezag.com/fy2025de/
Überblick:
Geschäftsjahr 2025:
- Umsatz: 312,0 Mio. € (VJ: 295,8 Mio. €)
- bereinigtes EBIT: 77,7 Mio. € (VJ: 65,9 Mio. €)
- Nettogewinn: 48,8 Mio. € (VJ: 33,3 Mio. €)
Jahresprognose 2026:
- Umsatz von rund 320 Mio. €
- bereinigtes EBIT von rund 80 Mio. €
Über Eckert & Ziegler.
Die Eckert & Ziegler SE gehört mit über 1.000 Mitarbeitern zu den führenden Anbietern von isotopentechnischen Komponenten für Nuklearmedizin und Strahlentherapie. Das Unternehmen bietet weltweit an seinen Standorten Dienstleistungen und Produkte im Bereich der Radiopharmazie an, von der frühen Entwicklung bis hin zur Kommerzialisierung. Die Eckert & Ziegler Aktie (ISIN DE0005659700) ist im TecDAX der Deutschen Börse gelistet.
Wir helfen zu heilen.
forschen, produzieren, heilen / 23.03.2026
Einstein Center for Early Disease Interception eröffnet

Sie wollen Krankheiten erkennen, bevor Symptome entstehen: Im Einstein Center for Early Disease Interception bündeln Forschende von zwölf Berliner Institutionen ihre Expertise, um neue Wege der Prävention zu erschließen und schneller in die Anwendung zu bringen. Mit einem feierlichen Auftakt nimmt es heute seine Arbeit auf.
Gemeinsame Pressemitteilung von Max Delbrück Center, Charité – Universitätsmedizin Berlin, Berlin Institute of Health in der Charité, Technische Universität Berlin
Dass sich eine ernste Erkrankung anbahnt, bleibt oft jahrelang unbemerkt. Wenn Symptome auftreten, sind Organschäden bereits angerichtet und nur begrenzt rückgängig zu machen. Manchmal fehlt jeder Hebel, um den weiteren Verlauf zu stoppen.
Forschende aus zwölf führenden Berliner Institutionen wollen das ändern und Prävention neu denken. Mithilfe neuester Technologien – darunter Entwicklungen aus Berlin – wollen sie verstehen, was ganz am Anfang einer Erkrankung in den Zellen unseres Körpers geschieht. Dieses Wissen schafft die Grundlagen, um deutlich früher einzugreifen: in einem Stadium, in dem erst einzelne Zellen betroffen sind und die Krankheit noch steuerbar ist.
Die Forschenden bündeln ihre Expertise im „Einstein Center for Early Disease Interception“ (EC-EDI). Es wird heute feierlich mit Gästen aus Politik, Wissenschaft und Gesellschaft am Berliner Institut für medizinische Systembiologie des Max Delbrück Center in Mitte eröffnet. Die Einstein Stiftung Berlin fördert das Einstein-Zentrum mit insgesamt sechs Millionen Euro und unterstützt das EC-EDI bei der Rekrutierung junger internationaler Talente mit weiteren Mitteln, die das Land Berlin bereitstellt. Das Zentrum baut auf einer zweijährigen Vormodulphase auf.
Ein dynamisches Netzwerk für Schlüsseltechnologien
In den nächsten sechs Jahren werden die Wissenschaftlerinnen und Wissenschaftler die Entwicklung, Integration und Anwendung der Schlüsseltechnologien vorantreiben. Dazu gehören zum Beispiel Einzelzell-Multiomik-Technologien und räumliche Biologie, patient*innenspezifische Organoide, 3D-Bioprinting sowie Modellierungen von Mechanismen und Krankheitsverläufen auf der Basis von künstlicher Intelligenz. Es soll außerdem eine Plattform für die institutionenübergreifende Zusammenarbeit entstehen, um Forschungsergebnisse gemeinsam mit Unternehmen und Investor*innen schneller in die Klinik zu bringen und gleichzeitig gesellschaftlichen und wirtschaftlichen Mehrwert für Berlin zu schaffen. Im Fokus stehen zunächst Atemwegs- und neurologische Erkrankungen, wie beispielsweise entzündliche Lungenerkrankungen, Tuberkulose, Alzheimer und Multiple Sklerose.
Im EC-EDI arbeiten unter anderem die Charité – Universitätsmedizin Berlin, das Berlin Institute of Health in der Charité (BIH), das Max Delbrück Center, die Technische Universität Berlin, die Freie Universität Berlin, die Humboldt-Universität zu Berlin sowie weitere außeruniversitäre Einrichtungen wie das Museum für Naturkunde und Max-Planck-Institute zusammen.
Die vier Sprecher*innen zur Eröffnung
Professor Nikolaus Rajewsky (Hauptansprechperson; Direktor des Berliner Instituts für Medizinische Systembiologie des Max Delbrück Center und Professor an der Charité):
„Wir treiben eine molekulare Prävention und Intervention voran – und wollen sie möglichst schnell in die Klinik bringen. Große Fortschritte entstehen weder allein in der Klinik noch ausschließlich im Labor oder am Computer. Das Einstein-Zentrum schafft daher eine gemeinsame, offene Plattform mit klaren Regeln und kurzen Wegen. Kliniker*innen, Grundlagenforscher*innen und Datenwissenschaftler*innen arbeiten institutionenübergreifend, auch mit Unternehmen und Investor*innen, zusammen. Das macht uns schneller und trägt hoffentlich dazu bei, Berlin als international renommierten Standort und Akteur in diesem Gebiet weiterzuentwickeln.“
Professor Leif Erik Sander (Projektleiter; Direktor der Klinik für Infektiologie und Intensivmedizin an der Charité und Arbeitsgruppenleiter am BIH):
„Herkömmliche Methoden können oft die frühen Vorzeichen sich anbahnender Erkrankungen nicht erfassen. Zudem verstehen wir auch gar nicht immer, was eigentlich molekular schiefläuft und wie man kausal eingreifen könnte, um die Krankheiten zu stoppen. Hier setzt ‚Early Disease Interception‘ an: Mithilfe hochauflösender Technologien wollen wir verstehen, was die Weichen falsch stellt, und Möglichkeiten schaffen, diese Weichen sehr früh wieder umzustellen. Der Zug soll quasi zurück aufs gesunde Gleis. Aus unseren Erkenntnissen wollen wir innovative Lösungen, beispielsweise neue diagnostische Tests und Medikamente, entwickeln. So entsteht aus Forschung medizinischer Fortschritt und Wertschöpfung – und das stärkt den Innovations- und Wirtschaftsstandort Berlin.“
Dr. Janine Altmüller (Leiterin der Core Unit Genomics am Berlin Institute of Health in der Charité, BIH):
„Neue Methoden sind der Schlüssel zur Vision des Einstein-Zentrums: Noch nie zuvor war es möglich, charakteristische Merkmale wie Nukleinsäuren oder Proteine einzelner Zellen in ihrem natürlichen Gewebeverband so präzise und hochauflösend zu untersuchen. Selbst kleinste Veränderungen, die am Beginn einer Erkrankung stehen, können heute digitalisiert zum Beispiel mithilfe von KI besser entschlüsselt und besser verstanden werden. Dieses Wissen ist entscheidend, um gezielte Interventionen zu entwickeln. Im Einstein-Zentrum arbeiten Expertinnen und Experten aus unterschiedlichen Disziplinen gemeinsam an diesem Ziel und beschleunigen so die Translation wissenschaftlicher Erkenntnisse in die klinische Anwendung.“
Professor Jens Kurreck (Geschäftsführender Direktor des Instituts für Biotechnologie, Technische Universität Berlin):
„Das Einstein Center for Early Disease Interception eröffnet eine einzigartige Plattform für die enge Zusammenarbeit führender Berliner Forschungseinrichtungen und ermöglicht es, an verschiedenen humanen Modellen frühe Mechanismen der Krankheitsentstehung besser zu verstehen. Besonders wichtig ist dabei, jungen Wissenschaftlerinnen und Wissenschaftlern im Rahmen dieses Konsortiums Zugang zu modernsten Technologien zu bieten und ihnen optimale Bedingungen für den Aufbau ihrer wissenschaftlichen Karrieren zu schaffen.“
Weiterführende Informationen
forschen, produzieren, heilen / 19.03.2026
Internationale Zusammenarbeit bei klinischen Studien intensivieren

Im Rahmen der Australian Clinical Trials Initiative (ACTI) besuchten heute australische Unternehmen und Vertreter der Australien Government’s Trade and Invest Commission den Wissenschafts- und Biotechcampus Berlin-Buch. Die Initiative wirbt für Australien als attraktiven Standort für klinische Studien.
Dr. Christina Quensel, CEO der Campus Berlin-Buch GmbH, begrüßte die Gäste und informierte auf einem Rundgang über das Ökosystem des Campus aus biomedizinischer Grundlagen- und klinischer Forschung, Life Science Start-ups und Biotechnologie-Unternehmen, die hier in einem der führenden Biotechparks in Europa arbeiten.
Die Delegation erhielt einen Einblick in zwei wissenschaftliche Core Facilities: das Proteomic Lab des Berlin Institute of Health in der Charité und die Kryo-Elektronenmikroskopie, eine kooperative wissenschaftliche Infrastruktur der Charité – Universitätsmedizin Berlin, des Max Delbrück Center und des Leibniz-Forschungsinstituts für Molekulare Pharmakologie.
Im Gründerzentrum BerlinBioCube besuchten die australischen Gäste die Start-ups CheckImmune GmbH, einer CRO, und T-knife GmbH, ein pharmazeutisches Unternehmen, das hochinnovative Krebstherapien entwickelt.
Bei einem Networking Lunch tauschte sich die Delegation intensiv mit Geschäftsführenden und Akteuren des BiotechParks Berlin-Buch aus.
Herzlichen Dank an unsere Gäste!
Minesh Lalla, Senior Business Development Manager at Peter MacCallum Cancer Centre (CTS)
Jason Erasmus, Business Development Manager at Beyond Drug Development (CRO)
Tim Vale, Business Development Manager at Resolian Bioanalytics (Lab)
Karl Boehle, Senior Business Development Manager, Austrade
Pallavi Mishra, South Australia Trade & Investment Manager, Austrade
George Zafiris MBA, Prime Financial Group (R&D Tax Advisors)
Bellberry (Ethics)
Im Anschluss ging es für die Delegation weiter zu Berlin Partner für Technologie und Wirtschaft, die in Kooperation mit Austrade zu einem exklusiven Seminar zu Möglichkeiten der deutsch-australischen Zusammenarbeit bei klinischen Studien eingeladen hatten. Die Veranstaltung beleuchtete, wie das australische Ökosystem für klinische Studien aufgebaut ist und welche wesentlichen Stärken und Effizienzvorteile es bietet. Eingeladen waren Führungskräfte aus den Bereichen Forschung und Entwicklung in der Pharma- und Biotech-Branche, Entscheidungsträger für klinische Abläufe und Studienstrategien, Auftragsforschungsinstitute (CROs) und Anbieter klinischer Dienstleistungen, Führungskräfte aus Hochschulen, Krankenhäusern und Forschungseinrichtungen sowie Akteure aus Politik und dem Innovations-Ökosystem.
forschen / 17.03.2026
Körperfett fördert Entzündungen im Darm
Fettgewebe rund um den Darm verstärkt die Entzündungen bei Morbus Crohn. Das berichten Forschende des Max Delbrück Center und der Charité – Universitätsmedizin Berlin im „Journal of Clinical Investigation“. Außerdem erklären sie, wie Mutationen in Immunzellen zu der Krankheit beitragen können.
Morbus Crohn ist eine chronisch-entzündliche Erkrankung des Darms, von der weltweit Millionen von Menschen betroffen sind. Ein auffälliges Merkmal der Krankheit ist das „schleichende Fett“: Fettgewebe, das sich um entzündete Darmabschnitte legt. Forschende vermuten seit langem, dass dieses Gewebe den Krankheitsverlauf beeinflussen kann. Die zugrunde liegenden Mechanismen sind bislang aber unklar.
Wissenschaftler*innen der Charité – Universitätsmedizin Berlin und des Berliner Instituts für Medizinische Systembiologie am Max Delbrück Center (MDC-BIMSB) berichten jetzt gemeinsam mit weiteren Kolleg*innen im „Journal of Clinical Investigation“, dass das Fettgewebe Signale aussendet, die letztendlich die Darmbarriere bei Morbus Crohn schädigen. Zudem zeigen sie, dass im Laufe des Lebens erworbene Mutationen im Erbgut von Immunzellen die Krankheit begünstigen können.
„Es ist schon lange bekannt, dass ein Zusammenhang zwischen Adipositas und Morbus Crohn besteht“, sagt Professorin Ashley Sanders, die Leiterin der Arbeitsgruppe „Genominstabilität und somatischer Mosaizismus“ am MDC-BIMSB und eine der Letztautor*innen der Studie. „Es ist zwar durchaus bekannt, dass Fettgewebe molekulare Signale aussendet, die Entzündungen begünstigen. In unserer Studie beschreiben wir aber den Zusammenhang zwischen diesen aus dem Fettgewebe stammenden Signalen und Entzündungen im Darm wirklich im Detail.“
Mäuse ohne Fettgewebe
Die Forschenden führten zunächst Versuche an einem Mausmodell für generalisierte Lipodystrophie durch – einer sehr seltenen Erkrankung, bei der den Betroffenen unter anderem Fettgewebe fehlt. Setzte das Team die Mäuse einer chemischen Substanz aus, die normalerweise Darmentzündungen verursacht, stellten sie fest, dass die Mäuse mit Lipodystrophie widerstandsfähiger waren als ihre Artgenossen. Ihre Darmbarriere blieb stabil und sie wiesen geringere Mengen an entzündungsfördernden Immunzellen auf. Insbesondere die Zahl der Th1- und Th17-T-Zellen – das sind spezialisierte Immunzellen, die Abwehrreaktionen koordinieren – war reduziert.
Transplantierten die Wissenschaftler*innen den Lipodystrophie-Mäusen Fettgewebe, waren die Tiere anfälliger für die chemisch ausgelöste Darmentzündung. Allerdings war dieser Effekt nur dann zu beobachten, wenn das transplantierte Fett Leptin produzieren konnte. Das deutet darauf hin, dass Leptin zumindest bei Mäusen eine zentrale Rolle bei der Regulierung des Immunsystems spielt.
„Diese Ergebnisse haben wir zwar erwartet, da frühere Forschungen bereits gezeigt hatten, dass Fettgewebe ein aktives Immunorgan ist“, sagt die Charité-Professorin Britta Siegmund, die ebenfalls eine Letztautorin der Studie ist. „Sie unterstreichen aber, dass Signale aus dem Fettgewebe entzündliche Reaktionen im Darm erheblich verstärken können.“
Rätselhafte klinische Befunde
Allerdings schienen die Ergebnisse im Widerspruch zu den Befunden eines klinischen Falls an der Charité zu stehen: Dort gab es eine erkrankte Person mit erworbener generalisierter Lipodystrophie, die zudem an Morbus Crohn erkrankt war, obwohl sie überhaupt kein Fettgewebe besaß. „Das war merkwürdig und wir wollten verstehen, warum dieser Mensch die Krankheit entwickelt hatte“, sagt Siegmund.
Mithilfe der Einzelzellsequenzierung untersuchte die Arbeitsgruppe von Sanders Immunzellen aus dem Blut und dem Darmgewebe der betroffenen Person. Das Team stieß auf eine ungewöhnlich große Gruppe von Zellen, die eine Mutation in einem Gen namens NRAS aufwiesen. Das Gen trägt zur Regulierung des Zellwachstums und des Zellüberlebens bei.
Der Befund deutete darauf hin, dass sich diese Zellen aus einer einzigen Zelle in einem Prozess, der als klonale Expansion bezeichnet wird, vermehrt hatten. Solche mutierten Zellen entstehen spontan und werden nicht vererbt. Zellen mit einem veränderten NRAS-Gen leben länger und teilen sich häufiger, als sie sollten – was möglicherweise zu chronischen Entzündungen führt.
„Die Mutation hat wahrscheinlich dazu beigetragen, dass die entzündungsfördernden T‑Zellen längere Zeit überleben und sich vermehren konnten“, erklärt Sanders. Diese anhaltende Vermehrung könnte die beobachteten systemischen und intestinalen Entzündungen begünstigt haben. „Darüber hinaus zeigen unsere Ergebnisse, wie leistungsfähig Einzelzell-Genomtechnologien sein können, um verborgene genetische Veränderungen in einzelnen Immunzellen aufzudecken“, fügt die Forscherin hinzu.
Für eine personalisierte Therapie
Neben entzündungsfördernden Signalen produziert das Fettgewebe weitere Botenstoffe – zum Beispiel Adipokine, zu denen auch das Leptin gehört, das vor allem für seine regulierende Wirkung auf Appetit und Stoffwechsel bekannt ist. In der Studie erhielt die Person mit Lipodystrophie eine synthetische Form von Leptin, um einen ebenfalls vorhandenen Typ-2-Diabetes zu behandeln. Das Hormon verbesserte zwar die Stoffwechselgesundheit, verstärkte jedoch gleichzeitig die entzündungsfördernde Signalübertragung und erhöhte die Anzahl der Th17-Immunzellen.
„Diese Erkenntnis verdeutlicht, wie Adipokine wie Leptin und Mutationen in Immunzellen zusammenwirken und so chronische Entzündungskrankheiten beeinflussen“, sagt Professor Carl Weidinger von der Charité, ein weiterer Letztautor der Studie. Das Zusammenspiel von Stoffwechsel- und genetischen Faktoren könne möglicherweise erklären, warum sich Morbus Crohn bei verschiedenen Menschen unterschiedlich äußere, fügt Weidinger hinzu. „Wenn wir diese Wechselwirkungen verstehen, können wir hoffentlich präzisere, personalisierte Behandlungsansätze entwickeln.“
Text: Gunjan Sinha
Weitere Informationen
Genome Instability and Somatic Mosaicism
Genominstabilität und somatischer Mosaisizmus
Literatur
Marilena Letizia, Toka Omar, Patrick Weidner et al. (2026): „Characterization of intestinal immune responses in generalized human and murine lipodystrophy“. Journal of Clinical Investigation, DOI: 10.1172/JCI192322
Bild
Das Bild zeigt Darmgewebe aus einem Mausmodell für die erworbene generalisierte Lipodystrophie. Das Gewebe blieb auch nach der Behandlung mit einer Chemikalie, die normalerweise eine Darmentzündung auslöst, intakt.
leben / 16.03.2026
Bebauungsplan 3-89 für das Neue Stadtquartier Elisabeth-Aue in Pankow - Bürgerinnen und Bürger sind aufgerufen ihre Stellungnahme abzugeben
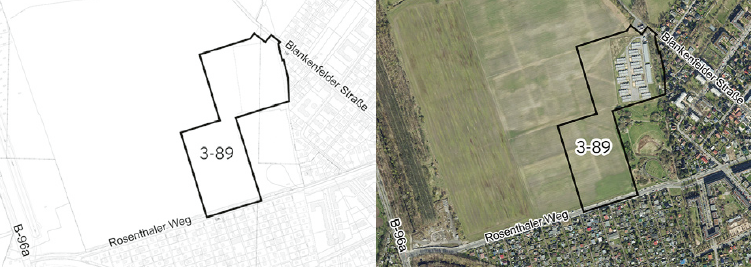
Vom 16.März bis einschließlich 20. April 2026 findet die öffentliche Auslegung zum Entwurf des Bebauungsplans 3-89 (Elisabeth-Aue, Teilprojekt 1) im Bezirk Pankow, Ortsteil Blankenfelde, statt. Die Beteiligung der Öffentlichkeit ist der letzte formelle Schritt vor den abschließenden Abstimmungen in den parlamentarischen Gremien und dem Festsetzungsbeschluss.
Das Neue Stadtquartier Elisabeth-Aue gehört zu den großen Wohnungsbauvorhaben Berlins. Es ist eines der insgesamt 24 Neuen Stadtquartiere, in denen stadtweit bezahlbarer Wohnraum und soziale Infrastruktur wie Kitas und Schulen geschaffen wird. Das Projekt wird nach Fertigstellung von den landeseigenen Wohnungsbaugesellschaften HOWOGE und Gesobau mitpreisgebunden vermietet. Etwa 870 Wohnungen, eine Oberschule mit entsprechenden Sport,- Frei- und sonstigen Flächen, öffentliche Grünflächen sowie öffentliche Straßenverkehrsflächen werden auf der Teilfläche 1 (B-Plan 3-89) entstehen und sorgen so für ein attraktives neues Zuhause in Berlin.
Vom 16.03.2026 bis einschließlich 20.04.2026 kann der Entwurf des Bebauungsplans 3-89 im Internet eingesehen werden, um sich über Ziele, Zwecke und Auswirkungen der Planung zu informieren und eine Stellungnahme abzugeben.
Zusätzlich zur Veröffentlichung im Internet werden die nach § 3 Abs. 2 Satz 1 BauGB zu veröffentlichenden Unterlagen in Form einer öffentlichen Auslegung in dem genannten Zeitraum von Montag bis Donnerstag 09:00 bis 17:00 Uhr, Freitag 09:00 bis 16:00 Uhr sowie nach telefonischer Vereinbarung unter 90173-3856/-4233 oder nach Terminvereinbarung per E-Mail (3-89@senstadt.berlin.de) in der Senatsverwaltung für Stadtentwicklung, Bauen und Wohnen, Württembergische Straße 6, 10707 Berlin, Raum 006 zur Verfügung gestellt.
Ebenfalls einsehbar sind die Unterlagen in dem genannten Zeitraum von Montag bis Freitag 09:00 bis 18:00 Uhr im Bezirksamt Pankow in der Storkower Str. 97, 10407 Berlin, im Erdgeschoss im Foyer zur rechten Seite.
Die während der Auslegungsfrist abgegebenen Stellungnahmen werden mit den anderen öffentlichen und privaten Belangen abgewogen.
Information und Beteiligung ist über folgenden Link möglich: https://be.beteiligung.diplanung.de/plan/3-89 & https://www.berlin.de/sen/stadtentwicklung/neue-stadtquartiere/elisabeth-aue/
forschen, heilen / 13.03.2026
Wie Krebs-Immuntherapien das Herz beeinflussen
Checkpoint-Inhibitoren helfen zwar gegen Krebs, erhöhen aber das Risiko für Herzleiden. Wie sich die Therapie sicherer gestalten lässt, untersucht ein interdisziplinäres Team, zu dem auch Forschende des Max Delbrück Center gehören. Die Hector Stiftung unterstützt das Projekt mit 1,3 Millionen Euro.
In der Krebstherapie haben Checkpoint-Inhibitoren seit ein paar Jahren ihren festen Platz. Die Antikörper stacheln das Immunsystem dazu an, vehementer gegen entartete Zellen vorzugehen. Vor allem Patient*innen mit schwarzem Hautkrebs, aber auch Lungen‑, Nieren- oder Blasenkrebs profitieren von der Immuntherapie oft mehr als von anderen Behandlungsoptionen.
Gut fürs Herz sind die Medikamente allerdings nicht. „Wir gehen davon aus, dass Krebspatientinnen und ‑patienten durch eine Immuntherapie mit Checkpoint-Inhibitoren ein etwa dreifach erhöhtes Risiko für Herzerkrankungen wie die Koronare Herzkrankheit haben“, sagt der Kardio-Onkologe Professor Lorenz Lehmann vom Universitätsklinikum Heidelberg. Gemeinsam mit einem interdisziplinären Team möchte Lehmann herausfinden, welche biologischen Mechanismen diese Nebenwirkungen hervorrufen – um die Therapie langfristig schonender fürs Herz zu machen.
Zu dem Konsortium namens ATHERIC-CARE (Atherosclerosis Risk in Cancer Patients after Immune Checkpoint-Inhibitor Therapy – Assessment and Exploration) gehören Dr. Isabel Poschke vom Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg, Dr. Henrike Maatz vom Max Delbrück Center in Berlin-Buch, Professorin Sylvia Saalfeld von der Universität Kiel und Professor Oliver Müller vom Universitätsklinikum Schleswig-Holstein (UKSH) in Kiel. Seit dem 1. Februar 2026 fördert die Hector Stiftung die Arbeit des multizentrischen Teams drei Jahre lang mit insgesamt 1,3 Millionen Euro.
Entzündete Herzkranzgefäße
Die Koronare Herzkrankheit ist eine Atherosklerose der Herzkranzgefäße. Blutfette und andere Substanzen aus dem Blut lagern sich dabei an den inneren Gefäßwänden ab und lösen dort chronische Entzündungen aus. Mit der Zeit verengen sich die Blutgefäße immer mehr, wodurch es zu Herzschwäche oder einem Herzinfarkt kommen kann. ATHERIC-CARE geht vor allem der Frage nach, wie Checkpoint-Inhibitoren diesen Entzündungsmechanismus aktivieren oder beschleunigen.
Die Wissenschaftler*innen untersuchen zum Beispiel anhand von DNA-Analysen, welche Immunzellen die Atherosklerose vorantreiben. In Tierexperimenten erforschen sie die Entzündungsmechanismen von Beginn an und mithilfe des maschinellen Lernens werten sie computertomographische Aufnahmen von Betroffenen aus. Denn diese Bilder spüren nicht nur im klinischen Alltag Metastasen auf, sondern können durch den Einsatz von KI auch Veränderungen an den Herzkranzgefäßen sichtbar machen.
„Unsere Aufgabe wird es sein, herauszufinden, welche Gene in den Zellen der Herzkranzgefäße und im umliegenden Gewebe aktiv werden – was also genau auf molekularer Ebene in den verschiedenen Zelltypen passiert“, sagt Henrike Maatz. Die Forscherin aus der Arbeitsgruppe „Genetik und Genomik von Herz-Kreislauferkrankungen“ von Professor Norbert Hübner am Max Delbrück Center wird dafür vor allem zwei Verfahren anwenden: die Einzelkern-RNA-Sequenzierung (single-nucleus RNA-sequencing, kurz snRNA-sec) und die Räumliche Transkriptomik (Spatial Transcriptomics).
Forschung für mehr Lebensqualität
„Wir möchten so zum Beispiel die Interaktion der Immunzellen mit den Endothelzellen, die die Blutgefäße von innen auskleiden, genauer charakterisieren“, erläutert Maatz. „Unser Ziel ist es, zu verstehen, wie die Immuntherapie T‑Zell-vermittelte Entzündungen in Blutgefäßen fördert, die instabile Gefäßablagerungen und Atherosklerose begünstigen können.“ Mithilfe der Räumlichen Transkriptomik wolle sie unter anderem herausfinden, wie die Immunzellen in den Plaques verteilt sind. Für ihre geplanten Arbeiten wird die Forscherin von der Hector Stiftung rund 286.000 Euro erhalten.
„Indem wir die Ergebnisse, die in den verschiedenen Forschungsbereichen des Konsortiums erzielt werden, zusammenführen, wollen wir Biomarker und Strategien identifizieren, die die Immuntherapie sicherer machen – und damit auch die Lebensqualität der Patientinnen und Patienten verbessern“, fasst der Projektleiter Lehmann die Ziele von ATHERIC-CARE zusammen.
Auf die bevorstehende Kooperation freut sich Maatz: „Gemeinsam werden wir natürlich viel mehr erreichen, als eine einzelne Arbeitsgruppe es tun könnte“, sagt sie. „Und mit Lorenz Lehmann haben wir auch schon in anderen Projekten sehr erfolgreich zusammengearbeitet.“
Weitere Informationen
heilen / 12.03.2026
Darmkrebsmonat März: Risikofaktor rotes Fleisch? Was Sie über Darmkrebs wissen sollten
Darmkrebs gehört zu den häufigsten Krebserkrankungen in Deutschland. Im Helios Klinikum Berlin-Buch werden jedes Jahr über 100 Patient:innen mit Darmkrebs operiert und behandelt. Anlässlich des Darmkrebsmonats März informiert Prof. Dr. med. Roger Wahba, Chefarzt der Allgemein-, Viszeral- und Onkologischen Chirurgie am Helios Klinikum Berlin-Buch, über die Bewertung von rotem und verarbeitetem Fleisch als Risikofaktor und ordnet die Erkenntnisse im Kontext der Darmkrebsprävention ein.
Bereits 2015 hat die Internationale Agentur für Krebsforschung (IARC), eine Einrichtung der Weltgesundheitsorganisation (WHO), rotes Fleisch als wahrscheinlich krebserregend (Gruppe 2A) und Fleischwaren als krebserregend (Gruppe 1) eingestuft. Unter rotem Fleisch versteht man das Muskelfleisch von Säugetieren wie Rind, Schwein oder Lamm. Als Fleischwaren gelten hingegen alle Produkte, in welchen Fleisch durch Pökeln, Räuchern, Salzen oder andere Verfahren verarbeitet und haltbar gemacht wurden, wie etwa Wurst, Schinken oder getrocknetes Fleisch.
Darmkrebs ist eine der häufigsten Krebsarten in Deutschland. Epidemiologische Auswertungen deuten darauf hin, dass der regelmäßige Konsum von verarbeitetem Fleisch mit einem erhöhten Darmkrebsrisiko verbunden ist: Der tägliche Verzehr von 50 Gramm verarbeitetem Fleisch erhöht das Risiko für Darmkrebs um 18 Prozent. Für rotes Fleisch wurde bei einer täglichen Aufnahme von 100 Gramm ein Anstieg des Darmkrebsrisikos um 17 Prozent festgestellt (Lancet Oncology 2015; doi: 10.1016/S1470-2045(15)00444-1). Das bestätigt auch Prof. Dr. med. Roger Wahba, Chefarzt der Allgemein-, Viszeral- und Onkologischen Chirurgie am Helios Klinikum Berlin-Buch: „Es zeigt sich, dass der Verzehr von rotem und vor allem verarbeitetem Fleisch mit einer erhöhten Inzidenz von Darmkrebs in Zusammenhang steht. Das ist insbesondere auf die sekundären krebserzeugenden Stoffe zurückzuführen“. Diese entstehen hauptsächlich bei der Zubereitung unter hohen Temperaturen, wie beim Braten oder Grillen von Fleisch und Fleischwaren, aber auch bei der industriellen Verarbeitung.
Wichtig ist: Bei dieser Einschätzung handelt es sich um eine Risikobewertung auf Bevölkerungsebene. Ein eindeutiger Ursache-Wirkungs-Nachweis für den Einzelfall lässt sich daraus nicht ableiten. Gleichwohl zeigt sich, dass in Gesellschaften mit traditionell hohem Fleischkonsum die Darmkrebsinzidenz höher ist als in Regionen mit überwiegend pflanzenbasierter Ernährung. Auch Ernährungsempfehlungen wie die Ernährungspyramide tragen dieser Einschätzung zunehmend Rechnung. Orientierung bietet eine pflanzenbetonte Kost: Ein großer Anteil der täglichen Ernährung sollte aus Gemüse, Obst, Vollkornprodukten und Hülsenfrüchten bestehen.
Im Helios Klinikum Berlin-Buch behandelt das Team der Allgemein-, Viszeral- und Onkologischen Chirurgie hoch spezialisiert Patient:innen mit Darmkrebserkrankungen. Ein Schwerpunkt liegt dabei auch auf der Behandlung des Darmkrebses gerade auch ohne Operation. Für Darmkrebspatient:innen empfiehlt das Team eine ballaststoffreiche, pflanzenbasierte Ernährung; vor, während und nach einer Darmkrebsoperation. „Beobachtungsstudien deuten darauf hin, dass ein gesunder Lebensstil und eine Umstellung der Ernährung hin zu mehr pflanzlichen Lebensmitteln mit einer günstigeren Prognose assoziiert sein kann“, so Prof. Dr. med. Roger Wahba.
Neben der Ernährung ist auch das Alter ein wesentlicher Risikofaktor: Mit zunehmendem Alter steigt die Darmkrebsinzidenz an, besonders zwischen 70 bis 80 Jahren. Langjährige Ernährungs- und Lebensstilgewohnheiten könnten hierzu beitragen. Ob und in welchem Ausmaß der Wandel hin zur stärker pflanzenbasierten Ernährung künftig die Zahl der Neuerkrankungen an Darmkrebs beeinflusst, wird sich erst mit zeitlichem Abstand zeigen.
Gleichzeitig ist Darmkrebsprävention auch für junge Menschen relevant. „Diese können gerade im Sinne der Primärprävention mit der Anpassung ihrer Ernährung, regelmäßiger Bewegung und dem Wahrnehmen von Vorsorgeuntersuchungen ihr persönliches Risiko aktiv beeinflussen“, betont Prof. Dr. med. Wahba. Um dieser Entwicklung Rechnung zu tragen, baut das Helios Klinikum Berlin-Buch künftig sein Angebot für jüngere Menschen aus und plant spezielle Informations- und Vorsorgeformate.
Zusätzlich kann die Reduktion des Konsums von rotem und verarbeitetem Fleisch nicht nur gesundheitliche Vorteile bieten, sondern auch zur Verringerung der Treibhausgasemissionen beitragen. Auch diese Dimension sollte im Sinne der Nachhaltigkeit nicht vernachlässigt werden und behält ihre Relevanz über den Darmkrebsmonat März hinaus.
Das Helios Klinikum Berlin-Buch ist ein modernes Krankenhaus der Maximalversorgung mit über 1.000 Betten in mehr als 60 Kliniken, Instituten und spezialisierten Zentren sowie einem Notfallzentrum mit Hubschrauberlandeplatz. Jährlich werden hier mehr als 55.000 stationäre und über 144.000 ambulante Patienten mit hohem medizinischem und pflegerischem Standard in Diagnostik und Therapie fachübergreifend behandelt, insbesondere in interdisziplinären Zentren wie z.B. im Brustzentrum, Darmzentrum, Hauttumorzentrum, Perinatalzentrum, der Stroke Unit und in der Chest Pain Unit. Die Klinik ist von der Deutschen Diabetes Gesellschaft als „Klinik für Diabetiker geeignet DDG“ zertifiziert. Zudem ist die Gefäßmedizin in Berlin-Buch dreifach durch die Fachgesellschaften der DGG (Deutsche Gesellschaft für Gefäßchirurgie und Gefäßmedizin), der DGA (deutsche Gesellschaft für Angiologie) und der DEGIR (deutsche Gesellschaft für interventionelle Radiologie) als Gefäßzentrum zertifiziert.
Gelegen mitten in Berlin-Brandenburg, im grünen Nordosten Berlins in Pankow und in unmittelbarer Nähe zum Barnim, ist das Klinikum mit der S-Bahn (S 2) und Buslinie 893 oder per Auto (ca. 20 km vom Brandenburger Tor entfernt) direkt zu erreichen.
Fresenius Helios ist der führende private Gesundheitsdienstleister in Europa und versorgt mit rund 140 Kliniken und zahlreichen ambulanten Einrichtungen jährlich rund 27 Millionen Menschen. Zusammen mit Fresenius Kabi, Anbieter von Gesundheitsprodukten für kritisch und chronisch Kranke, gehört Fresenius Helios zum Gesundheitskonzern Fresenius. Mit seinen rund 130.000 Mitarbeitenden der Helios Gruppe in Deutschland sowie Quirónsalud in Spanien und Lateinamerika erzielte Fresenius Helios 2025 einen Gesamtumsatz von mehr als 13,5 Milliarden Euro.
In Deutschland betreibt Helios mehr als 80 Kliniken, rund 200 Medizinische Versorgungszentren (MVZ), sechs Präventionszentren und 30 arbeitsmedizinische Zentren. Helios behandelt im Jahr 2025 rund 5,6 Millionen Menschen in Deutschland, davon mehr als 4 Millionen ambulant. Seit seiner Gründung setzt Helios auf messbare, hohe medizinische Qualität und Datentransparenz und ist bei über 90 Prozent der Qualitätsziele besser als der bundesweite Durchschnitt. In Deutschland beschäftigt Helios rund 80.000 Mitarbeitende und erwirtschaftete im Jahr 2025 einen Umsatz von rund 8,1 Milliarden Euro. Helios steht mit 35 eigenen Bildungszentren für Aus-, Fort- und Weiterbildung im Gesundheitswesen. Sitz der Unternehmenszentrale ist Berlin.
Quirónsalud verfügt über 57 Kliniken, davon sieben in Lateinamerika, rund 130 ambulante Gesundheitszentren sowie über 300 Einrichtungen für betriebliches Gesundheitsmanagement. Jährlich werden hier rund 22 Millionen Patient:innen behandelt, davon mehr als 20 Millionen ambulant. Quirónsalud beschäftigt rund 50.000 Mitarbeitende und erwirtschaftete 2025 einen Umsatz von mehr als 5,4 Milliarden Euro.
leben / 11.03.2026
Jetzt FEIN-Mittel für ehrenamtliche Arbeit beantragen - 78.900 Euro stehen zur Verfügung
Ehrenamtliche Initiativen und Projekte, die bei der Verbesserung der öffentlichen Infrastruktur des Bezirks Pankow helfen wollen, können ab sofort finanzielle Unterstützung beim Bezirksamt beantragen. Dem Bezirk stehen hierfür 78.900 Euro aus Mitteln der Senatsverwaltung für Stadtentwicklung, Bauen und Wohnen im Rahmen des Projekts Freiwilliges Engagement in Nachbarschaften (FEIN) zur Verfügung. Die Verteilung dieser Mittel für die einzelnen Bereiche der öffentlichen Infrastruktur (Grünflächen, Jugendclubs, Schulen etc.) hat das Bezirksamt jetzt beschlossen.
Anträge können bis 10. April 2026 eingereicht werden
Gefördert werden die Aufwertung und Verbesserung von Schulen, Sportflächen, Kitas, Jugendclubs, öffentlichen Spielplätzen, Senioren- und Stadtteilzentren, Nachbarschaftstreffs, Selbsthilfekontaktstellen, öffentlichen Straßen und Plätzen sowie Grünflächen. Formlose Anträge können per Post bis einschließlich Freitag, den 10. April 2026 bei den Abteilungen oder im Büro der Bezirksbürgermeisterin im Rathaus Pankow, Breite Straße 24A-26, 13187 Berlin, oder per E-Mail: bzbmstab@ba-pankow.berlin.deeingereicht werden.
Was wird gefördert?
Gefördert werden vorrangig Renovierungen, Reparaturen, Pflanzungen und ähnliche Arbeiten, für die notwendige Sachmittel benötigt werden. Die Mittel müssen unter Angabe von Zweck, Art, Umfang, Zeitrahmen und Kosten beantragt werden. Zur zügigen Bearbeitung sind unbedingt die IBAN und BIC der Mittelempfänger sowie die Telefonnummer, unter der diese tagsüber zu erreichen sind, mitzuteilen.
Weitere Informationen zum Projekt Freiwilliges Engagement in Nachbarschaften (FEIN):
https://www.berlin.de/ba-pankow/ueber-den-bezirk/ehrenamtliches-engagement/artikel.708426.php
heilen / 10.03.2026
Qualität entscheidet: Helios Kliniken im Cluster Berlin-Brandenburg liefern medizinische Spitzenergebnisse

Helios kann mit seiner medizinischen Qualität überzeugen. Die nun für 2025 veröffentlichten Qualitätszahlen zeigen: Patient:innen erhalten bei Helios eine Versorgung auf höchstem Niveau.
Welches Krankenhaus bietet die beste Behandlung für mich oder meine Angehörigen? Entscheidend für die Antwort sind verlässliche und transparente Informationen über die Qualität medizinischer Leistungen. Ergebnisqualität ist für Helios seit über 25 Jahren gelebter Standard und folgt dem Dreiklang: flächendeckend und konsequent messen, veröffentlichen, verbessern. Der Anspruch: Für jedes medizinische Ziel will Helios besser sein als der Bundesdurchschnitt.
Wie sieht es aus im Helios Cluster Berlin-Brandenburg?
„Helios geht seinen Weg der Spezialisierung in Clustern und der transparenten Veröffentlichung von Qualitätsdaten konsequent weiter. Im Cluster Berlin-Brandenburg (Berlin-Buch, Emil von Behring, Bad Saarow) konnten wir 2025 alle medizinischen Ziele mit wenigen Ausnahmen erreichen. Dieses Ergebnis erstreckt sich über nahezu alle relevanten Fachbereiche und belegt die hohe Qualität der medizinischen Versorgung ebenso wie die Wirksamkeit der clusterbasierten Spezialisierungsstrategie“, sagt Cluster-Lead Carmen Bier.
Im standortübergreifenden Helios Cluster Berlin-Brandenburg wird eine medizinische Betreuung auf höchstem Niveau geboten. In allen Fachbereichen, dazu zählen beispielsweise die Kardiologie, die Onkologie und die Chirurgie, verbindet sich medizinische Expertise mit technologischer Exzellenz. Hochqualifizierte Spezialist:innen arbeiten interdisziplinär zusammen und gewährleisten so eine ganzheitliche Versorgung, die konsequent auf die Bedürfnisse der Patient:innen ausgerichtet ist.
Die Qualitätsergebnisse von Helios liegen seit Jahren bei rund 90 Prozent. 2025 erreichten sie mit knapp 92 Prozent sogar einen neuen Höchststand. Auch für die Zukunft nimmt sich Helios in Sachen Qualitätssteuerung einiges vor. Die klassische Messung blickt zurück. Künftig geht es stärker darum, klinische Daten näher am Behandlungsgeschehen zu nutzen und Risiken früher zu erkennen. Die Ergebnisqualität bleibt der Maßstab und wird daher immer weiter um digitale Unterstützung im laufenden Prozess ergänzt.
Über das Cluster Berlin-Brandenburg
Mit dem Clusteransatz verbessert Helios durch Bündelung von Kompetenz und Intensivierung des Netzwerkes die medizinische Qualität zum Wohle der Patient:innen. Zum Cluster Berlin-Brandenburg gehören das Helios Klinikum Berlin-Buch, das Helios Klinikum Emil von Behring und das Helios Klinikum Bad Saarow.
Weitere Informationen und Details im Internet unter www.helios-gesundheit.de/qualitaet
Das Helios Klinikum Berlin-Buch ist ein modernes Krankenhaus der Maximalversorgung mit über 1.000 Betten in mehr als 60 Kliniken, Instituten und spezialisierten Zentren sowie einem Notfallzentrum mit Hubschrauberlandeplatz. Jährlich werden hier mehr als 55.000 stationäre und über 144.000 ambulante Patienten mit hohem medizinischem und pflegerischem Standard in Diagnostik und Therapie fachübergreifend behandelt, insbesondere in interdisziplinären Zentren wie z.B. im Brustzentrum, Darmzentrum, Hauttumorzentrum, Perinatalzentrum, der Stroke Unit und in der Chest Pain Unit. Die Klinik ist von der Deutschen Diabetes Gesellschaft als „Klinik für Diabetiker geeignet DDG“ zertifiziert. Zudem ist die Gefäßmedizin in Berlin-Buch dreifach durch die Fachgesellschaften der DGG (Deutsche Gesellschaft für Gefäßchirurgie und Gefäßmedizin), der DGA (deutsche Gesellschaft für Angiologie) und der DEGIR (deutsche Gesellschaft für interventionelle Radiologie) als Gefäßzentrum zertifiziert.
Gelegen mitten in Berlin-Brandenburg, im grünen Nordosten Berlins in Pankow und in unmittelbarer Nähe zum Barnim, ist das Klinikum mit der S-Bahn (S 2) und Buslinie 893 oder per Auto (ca. 20 km vom Brandenburger Tor entfernt) direkt zu erreichen.
Das Helios Klinikum Emil von Behring in Berlin-Zehlendorf gehört zu den führenden medizinischen Einrichtungen der Region und bietet ein breites Spektrum an hochspezialisierter Medizin. Die Klinik für Orthopädie und Unfallchirurgie versorgt jährlich zahlreiche Patientinnen und Patienten mit modernsten Behandlungsmethoden und steht für eine qualitativ hochwertige, innovative und patientenorientierte Versorgung.
Das Helios Klinikum Bad Saarow ist ein Krankenhaus der qualifizierten Regelversorgung und gehört mit 629 Betten zu den modernsten und größten Kliniken der Region. 19 Fachabteilungen, drei Institute, eine Zentrale Notaufnahme, ein Zentrallabor und verschiedene zertifizierte Zentren ermöglichen ein umfassendes Spektrum modernster Diagnostik und innovativer Therapien. Insgesamt arbeiten am Klinikstandort und in den am Klinikum angeschlossenen medizinischen Einrichtungen etwa 1.300 Mitarbeiter:innen. Als Akademisches Lehrkrankenhaus der Medizinischen Hochschule Brandenburg Theodor Fontane nimmt das Klinikum an der Lehre und Ausbildung von Medizinstudenten teil.
Fresenius Helios ist der führende private Gesundheitsdienstleister in Europa und versorgt mit rund 140 Kliniken und zahlreichen ambulanten Einrichtungen jährlich rund 27 Millionen Menschen. Zusammen mit Fresenius Kabi, Anbieter von Gesundheitsprodukten für kritisch und chronisch Kranke, gehört Fresenius Helios zum Gesundheitskonzern Fresenius. Mit seinen rund 130.000 Mitarbeitenden der Helios Gruppe in Deutschland sowie Quirónsalud in Spanien und Lateinamerika erzielte Fresenius Helios 2025 einen Gesamtumsatz von mehr als 13,5 Milliarden Euro.
In Deutschland betreibt Helios mehr als 80 Kliniken, rund 200 Medizinische Versorgungszentren (MVZ), sechs Präventionszentren und 30 arbeitsmedizinische Zentren. Helios behandelt im Jahr 2025 rund 5,6 Millionen Menschen in Deutschland, davon mehr als 4 Millionen ambulant. Seit seiner Gründung setzt Helios auf messbare, hohe medizinische Qualität und Datentransparenz und ist bei über 90 Prozent der Qualitätsziele besser als der bundesweite Durchschnitt. In Deutschland beschäftigt Helios rund 80.000 Mitarbeitende und erwirtschaftete im Jahr 2025 einen Umsatz von rund 8,1 Milliarden Euro. Helios steht mit 35 eigenen Bildungszentren für Aus-, Fort- und Weiterbildung im Gesundheitswesen. Sitz der Unternehmenszentrale ist Berlin.
Quirónsalud verfügt über 57 Kliniken, davon sieben in Lateinamerika, rund 130 ambulante Gesundheitszentren sowie über 300 Einrichtungen für betriebliches Gesundheitsmanagement. Jährlich werden hier rund 22 Millionen Patient:innen behandelt, davon mehr als 20 Millionen ambulant. Quirónsalud beschäftigt rund 50.000 Mitarbeitende und erwirtschaftete 2025 einen Umsatz von mehr als 5,4 Milliarden Euro.
- News
- Termine
- Standortjournal „buchinside“
- Presseservice/Download
-
News Archiv
- Archiv News 2026
- Archiv News 2025
- Archiv News 2024
- Archiv News 2023
- Archiv News 2022
- Archiv News 2021
- Archiv News 2020
- Archiv News 2019
- Archiv News 2018
- Archiv News 2017
- Archiv News 2016
- Archiv News 2015
- Archiv News 2014
- Archiv News 2013
- Archiv News 2012
- Archiv News 2011
- Archiv News 2010
- Archiv News 2009
- Archiv News 2008








